شنبه 05 مهر 1399 کد خبر: 15

۱-مقدمه
در دنیای امروزی، با توسعه روزافزون فناوری نانو و ساخت محصولات مرتبط با آن، مواجهه با نانوذرات موجود در آلودگیهای آب، خاک، هوا، محیطهای کاری و آزمایشگاهی برای انسانها اجتنابناپذیر است. نانوذرات، ذرات جامدی هستند که به شیوه مایعات و گازها، توانایی جابهجایی، انتشار و تجمع در انواع بافتهای گیاهی و جانوری دارند[۱]. نانوذرات با تغییر در خصوصیات فیزیکوشیمیایی سطحی، برهمکنش فعالانهای با سلولهای بدن دارند. اجزای سلولی در معرض نانوذرات دچار تخریب، بدفرمی و نقص کارکردی شده و عملکرد زیستی سلولها مختل میشود[۲]. سلولهای یکسان، پاسخهای متفاوتی به انواع نانومواد با اندازه، شکل، بارسطحی مختلف میدهند و همینطور نانومواد مشابه، میتوانند پاسخهای سلولی متفاوتی در سلولهای مختلف ایجاد کنند. سمیت نانومواد بیشتر مربوط به ویژگیهایی از قبیل اندازه و نسبت سطح به حجم (عامل افزایش واکنشپذیری)، ترکیب شیمیایی (عامل اصلی واکنشپذیری) و بار سطحی (عامل واکنشهای الکترواستاتیکی) است[۳].
در حال حاضر مطالعات درمورد سمیت نانومواد در حال گسترش است وطیف وسیعی از اثرات حاد و مزمن نانوذرات بر رشد و متابولیسم موجودات زنده گزارش شدهاست. بسیاری از پژوهشگران معتقدند سمیت نانومواد باید قبل از بهکارگیری آنها مورد بررسی قرار بگیرد. در این مقاله بهطور خلاصه درمورد عوامل و فاکتورهای فیزیکی و شیمایی موثر بر واکنشپذیری و سمیتزایی نانوذرات بحث میشود.
۲- ویژگیهای موثر در سمیت نانومواد
سمیت نانوذرات، ناشی از تعامل خصوصیات فیزیولوژیکی ذرات نانومتری با سلولهای بدن است. به منظور استفاده ایمن در کاربردهای مختلف پزشکی، تکنولوژی و صنعت، بررسی مجموعهی خصوصیات و ویژگیهای موثر در سمیت بالقوه نانوذرات ضروری است. خصوصیاتی چون اندازه، ترکیب شیمیایی، شکل، ساختار سطح، پایداری، بار سطحی، آبدوستی یا آبگریزی، تجمع، گروههای عاملی شیمیایی، در برهمکنش نانوذرات با سلولهای بدن اثر میگذارند (شکل۱)[۴]. بر این اساس، با اصلاحات سطحی فیزیکی و شیمیایی میتوان نانوذرات زیستسازگار تولید کرد که برای تشخیص و درمان بیماریهای انسانی مورد استفاده قرار میگیرند[۵].
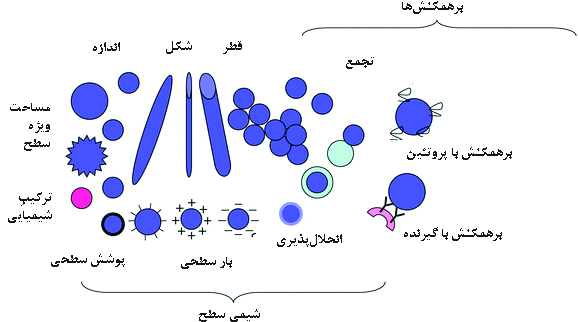
شکل۱- خصوصیات فیزیکوشیمیایی موثر در سمیت نانوذرات
۱-۲- اندازه ذرات
سلولهای پوششی بدن در قسمتهای حساس مثل مغز، جفت، کلیه با اتصالات قوی مثل یک سد درکنار هم قرار گرفتند تا از ورود مواد شیمیایی خطرناک به اندامهای ضروری جلوگیری کنند. ابعاد نانوذرات از اندازههای ۱ تا ۱۰۰ نانومتر، با گلوبولینهای پروتئینی به اندازه ۲ تا۱۰ نانومتر، مارپیچ DNA با قطر ۲ نانومتر و غشای سلولی با ضخامت ۱۰ نانومتر[۵] قابل مقایسه است. بنابراین نانوذرات به راحتی میتوانند مثل مولکولهای گاز از سدهای پوششی سلولی عبور کرده، وارد اندام ها[۶]، بافتها، سلولها و حتی اندامکهای مهمی چون هسته و میتوکندری شده و در آنجا رسوب کنند[۴].
نانوذرات با جذب سطحی برخی پروتئینها مثل ایمونوگلوبین، آلبومین و غیره، مجتمع و تشکیل توده میدهند. بسته به اندازهی توده و پس از اتصال به گیرندههای سطح غشای سلولها، از مسیرهای مختلف اندوسیتوز و پینوسیتوز وارد سلول میشوند.
بلورهای ادراری با اندازههای مختلف، در افراد سالم و بیماران سنگ کلیه وجود دارد. در یک آزمایش، جذب سلولی بلورهای منوهیدرات کلسیم اگزالات(COM) و دیهیدرات کلسیم اگزالات(COD) با اندازههای مختلف نانو و میکرو(۵۰ نانومتر، ۱۰۰ نانومترو ۱ میکرومتر) درسلولهای پوششی کلیوی با هم مقایسه شد. با توجه به نتایج این مطالعه، کاهش اندازه کریستالهای COD و COM در مکانیسم جذب سلولی از مسیرهای مختلف اندوسیتوز و ماکروپینوسیتوز اثر میگذارد. دو روش اندوسیتوز وابسته به کلاترین و اندوسیتوز وابسته به کاوئوله برای ورود بلورهای نانومتری به داخل سلول وجود دارد. بلورهای نانومتری COD و COM پس از ورود به سلول، با توزیع در لیزوزوم، یکپارچگی دیوارهی آن را از بین میبرد و در سلولها سمیت ایجاد میکنند(شکل۲). ماکروپینوسیتوز یک راه برای ورود بلورهای میکرومتری است که در اثر تغییرات رشتههای اکتین و برآشفتگی موضعی غشای سلول اتفاق میافتد[۲]. با مجموعهی این اطلاعات، میتوان روشی برای مهار جذب کریستالهای ادراری و جلوگیری از آسیبهای سلولی و تشکیل سنگکلیه پیدا کرد[۷].
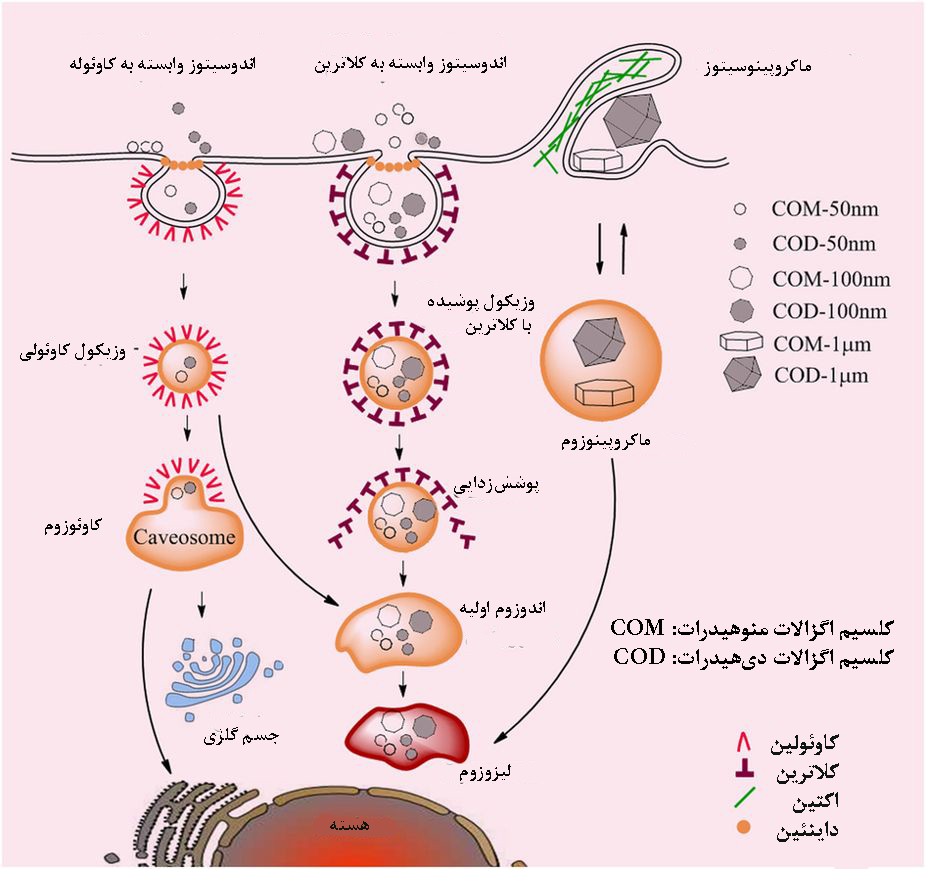
شکل۲- مسیرهای مختلف جذب سلولی بلورهای کلسیم اگزالات[۷]
با کوچک شدن اندازه ذرات، سطح بیشتری برای قرارگیری گروههای سطحی واکنشپذیر در دسترس قرار میگیرد. گروههای سطحی میتوانند آبدوست، آبگریز و یا دارای خواص کاتالیستی باشند[۳]. جذب موثر سلولی نانوذرات، با توجه به نسبت سطح وسیع و گروههای عاملی ویژه، افزایش مییابد. بر اساس یک مطالعه، نانوذرات طلا با اندازهی حداکثر ۶ نانومتر به راحتی وارد هسته میشوند. در حالیکه نانوذرات بزرگتر از آن (۱۶-۱۰نانومتر) فقط از غشای سیتوپلاسمی عبور کرده و در سیتوپلاسم یافت میشوند.
اندازه ذرات، تعیینکنندهی برهمکنش نانوذرات با سیستم گردش خون و ایمنی بدن است. این برهمکنش نیز، توزیع و تجمع ذرات در قسمتهای مختلف اندامهای بدن را تعیین میکند. آزمایشهای درونتنی[۱] نشان دادهاست که نانوذرات با اندازهی تقریبا ۲۵نانومتر، به صورت پینوسیتوز وارد سلول میشوند. نانوذرات کوچکتر از ۱۰نانومتر پس از تزریق به رگ، به سرعت در بین تمام اندامها و بافتها توزیع میشوند. درحالیکه نانوذرات بزرگتر (۲۵۰-۵۰ نانومتر) توسط سیستم ایمنی بدن شناسایی شده و از ورود آنها به درون بیشتر بافتها جلوگیری میشود[۵].
قرارگیری اتمها و مولکولهای بیشتر در سطح، منجر به بالا رفتن انرژی سطحی ذره، افزایش فعالیت شیمیایی و واکنشپذیری ذرات میشود. علت اصلی سمیت ذاتی نانوذرات، واکنشپذیری بالای آنها است[۴]. این تغییرات سطحی برهمکنش نانوذرات با اسکلت سلولی، رشتهDNA، اسیدهای چرب، کربوهیدرات و پروتئینهای سلولی را افزایش میدهد[۸]. بنابراین در سلولها، بدریختی، جهش ژنتیکی و اختلال در واکنشهای بیوشیمیایی ایجاد میشود که در نهایت دچار مرگ سلولی شده و سیستم ایمنی آنها را حذف میکنند[۶].
|
نکته: مولکولهای آلی و غیر آلی از راه اندوسیتوز وارد سلولها میشوند. اگر اندازهی ذرات کوچک و به صورت محلول باشد، پینوسیتوز و اگر اندازهی ذره بزرگ باشد و بهصورت ذرهای و جامد وارد سلول شود، اصطلاح فاگوسیتوز یا ذرهخواری به آن نسبت داده میشود. ماکروفاژهای بافتی و گلبولهای سفید با فرآیند فاگوسیتوز باکتریها را پاکسازی میکنند. |
۲-۲- شکل ذرات
نانوذرات در اشکال مختلفی مثل کره، میله، رشته، صفحه و هندسههای دقیقی چون هرم، مکعب، ششوجهی و غیره سنتز میشوند. برداشت ذرات توسط سلول و برهمکنش آنها با اجزای سلولی تا حد زیادی به شکل نانوذرات بستگی دارد. آسیب فیزیکی نانوذرات از حالت کروی به سمت شکلهای سوزنی و فیبری، مثلثی و زاویهدار افزایش مییابد (شکل۳)[۴]. برای مثال نانوکریستالهای سوزنی مثل کریستالهای اوریکاسید باعث آسیب سلولی و التهاب بافتی شدیدی میشوند. نانوصفحات اکسیدگرافن با آسیب فیزیکی به غشای سلولی در سطح سلولهای زنده سمیت ایجاد میکنند[۳].
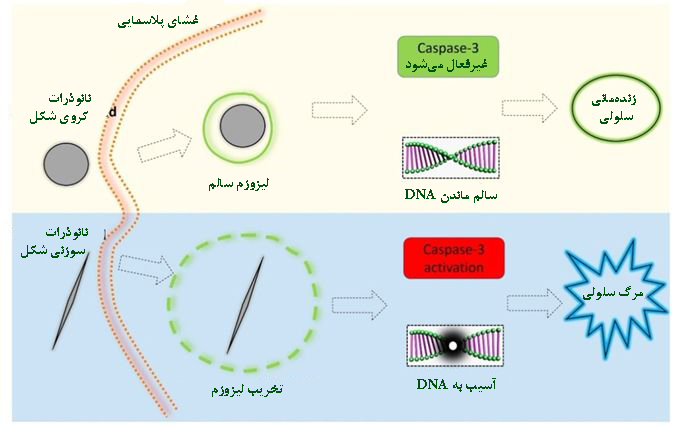
شکل۳- سمیت سلولی اشکال مختلف نانوذرات[۹]
از طرف دیگر نانوذرات کروی طلا با بیشترین نسبت طول به شعاع، نسبت به شکل نانومیله[۴] و یا رشته[۳] با سهولت و سرعت بیشتری از غشای سلولی عبور کرده و وارد سلول میشوند. بنابراین اشکال صفحهای، استوانهای و غیرکروی بهطور ذاتی کمتر از ذرات کروی جذب سلولهای ایمنی شده و به میزان بیشتر و مدت زمان طولانیتری در گردش خون جریان مییابند[۱۰].
ساختار بلوری نانوذرات بسته به محیط دچار تغییر میشود. برای مثال شبکه بلوری ZnS در تماس با آب و مایعات زیستی، به آرایش منظمتری درمیآیند. بنابراین سمیت نانوذرات به شکل ساختار بلوری مواد بستگی دارد. در یک مطالعه اثر نانوذرات اکسیدتیتانیوم (TiO2) با ساختارهای بلوری مختلف بر سلولهای لایه پوششی لولههای تنفسی انسان بررسی شد. با توجه به نتایج این آزمایش، نانوکریستال روتیلی (کریستالهای TiO2 با شکل منشوری) باعث آسیب اکسیداتیوDNA، اختلال در فرآیند میتوز و پراکسیداسیون لیپیدها میشوند. در حالیکه نانوکریستالهای آناتاز (بلورهایTiO2هشتوجهی) با اندازه یکسان، برای سلولها غیرسمی هستند[۵].
۳-۲- ترکیب شیمیایی
اگرچه سمیت نانوذرات به میزان زیادی به اندازه و شکل آنها بستگی دارد. اما ترکیب شیمیایی نانوذرات یکی دیگر از عوامل مهم موثر در سمیت است. نانوذرات اکسید سیلیکون و اکسید روی با اندازه یکسان ۲۰ نانومتری، در سلولهای موش آزمایشگاهی، مکانیسمهای سمیتزای متفاوتی دنبال میکنند. نانوذرات اکسید روی باعث ایجاد استرس اکسیداتیو میشوند. در حالیکه نانوذرات دیاکسید سیلیکون ساختار DNA را تغییر میدهند[۵]. درجدول۱، نانوذرات با ماهیتهای مختلف و ویژگیهای زیستی توصیفکننده اثرات سمی آنها مشخص شدهاست.
جدول۱-اثر ماهیت شیمایی نانوذرات بر سمیت[۱]
|
نانوذرات |
اندازه (نانومتر) |
فاکتورهای موثر در سمیت |
سازوکار سمیت |
|
نقره |
۱۵-۱۳ |
سمی بودن این عنصر به خواص سطح، رهاسازی ، پوشش نانوذرات نقره بستگی دارد. |
آسیب به غشای سلول، اختلال در همانندسازیDNA، حمله اکسیداتیو |
|
طلا |
۵-۴ |
مواجهه حاد و مزمن به لیگاندهای متصل بستگی دارد. |
اثر بر تولیدمثل دافنیا، پستانداران، جلبک و ماهی. تجمع در کبد و ایجاد استرس اکسیداتیو |
|
TiO2 |
۴۰-۱۰۰ |
سطح شیمیایی، پایداری، مکان قرار گرفتن، رهاسازی TiO2 در فاضلاب |
اثر منفی در رشد گندم و فعالیتهای آنزیمی خاک. اثرسمیت نوری و تکه تکه کردن DNA |
|
نانولولههای کربنی |
۲۰۰-۲۰ |
بستگی به اندازه ذرات، شکل، بار سطحی، تجزیه پذیری |
ریههای انسان، سلولهای پوششی، سمیت برای جنین، اختلال در تکثیر سلولی، آسیب به مغز، کبد، مغز و روده. سمیت تنفسی، سمیت نوری، اثر بر جوانهزنی بذر |
|
آمینوپلیاسترن |
۶۰-۲۰ |
سمیت با گروههای عاملی سطحی تعیین میشود. فرم کاتیونی سمیتر است. |
سمی برای ماکروفاژ، تومور کبدی، سلولهای پوششی، اندوتلیال رگها، جذب میتوکندری و مرگ سلولی |
|
نقاط کوانتومی |
کمتر از ۵۱۵ |
وابسته به تغییرات سطح، زیست فعالی، اندازه، غلظت، پایداری و عوامل محیطی |
استرس اکسیداتیو در گیاهان، سمیت اندوتلیال از طریق فعال شدن میتوکندریهای سلول |
یکی از مهمترین دلایل سمیت نانوذرات، تولید یونهای فلزی از هستهی نانوذرات است. ترکیب شیمیایی هستهی نانوذرات مثل Ag و Cd در حقیقت سمی است و به سلولها آسیب میزند. سایر یونهای فلزی مثل Fe و Zn، برای سلولها ضرری ندارند اما در غلظتهای بالا مشکلساز میشوند. بهتر است با پوستههای ضخیم پلیمری، لایههای سیلیس، پوستههای طلا و یا با استفاده از ترکیبات غیرسمی جلوی این اثر را گرفت. همچنین با افزودن برخی فلزات، میتوان ترکیب شیمیایی هسته را تغییر داده و با افزایش پایداری شیمیای، از نشت یونهای فلزی به بدن جلوگیری کرد[۵].
۴-۲- بار سطحی
غشای پلاسمایی سلولهای زنده به واسطهی برخی گلیکوپروتئینهای شارژ منفی و گروه آنیون فسفات در فسفولیپیدهای عرضغشایی، تمایل بیشتری برای جذب الکترواستاتیک نانوذرات با بار الکتریکی مثبت دارند[۵].
در یک مطالعه مشاهده شد که نانوذرات پلیاسترن با بار مثبت نسبت به بار منفی یا حالت خنثی، به طور موثرتری جذب سلولها شده و به شدت با رشتهی DNA که حاوی گروههای فسفات با بار منفی است، متصل شده و با آسیب به آن، باعث طولانی شدن فاز G1 و G0 چرخه سلولی میشود (شکل 4).نانوذرت طلا با بار مثبت به سرعت و میزان بیشتری وارد سلولهای خونی شده[۵]و بهنظر میرسد به راحتی جذب لیزوزومها میشوند و درنتیجه سمیت بیشتری نسبت به نانوذرات طلا با بارمنفی نشان میدهند[۳].
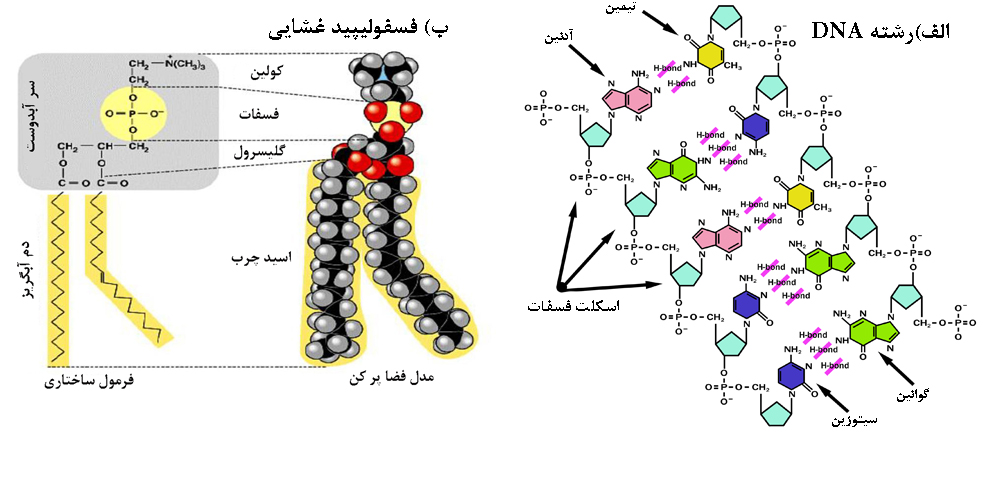
شکل۴- الف) رشته DNA حاوی گروههای قند، باز آلی و فسفات با بار منفی است. ب) فسفاتیدیل کولین یک فسفولیپید عرض غشایی با گروه آنیون فسفات [۵]
هرچقدر بار الکتریکی سطحی بیشتر باشد، سمیت آن نانوذره بیشتر است[۸]. نانوذرات کاتیونی با تمایل اتصالی به سلولهای ایمنی ماکروفاژ که حاوی گروه شیمیایی سیالیک اسید با بار منفی برروی سطح خود است[۲]، موجب تحریک و فعال شدن سیستم ایمنی بدن میشوند. درحالیکه نانوذرات آنیونی تمایل بیشتری برای تجمع در بافتهای توموری دارند[۴]. بنابراین، با تغییر بار نانوذرات میتوان رهاسازی و سمیت آنها را در بدن کنترل کرده و در سیستمهای موثر برای تحویل داروهای شیمیدرمانی به تودههای سرطانی استفاده کرد[۵].
بارسطحی نانومواد به عنوان یک عامل تعیینکننده رفتار کلوئیدی ذرات است و با تغییر شکل، اندازه و میزان تودهای شدن نانوذرات، به میزان قابل توجهی در پاسخهای سلولی اثر میگذارد. نانوذرات باردار در غلظتهای زیاد در عملکرد سد خونیـمغزی میتوانند اختلال ایجاد کنند[۳].
۵-۲- پوشش سطحی
خصوصیات نوری، مغناطیسی و الکتریکی سطحی[۵]، سازگاری، سرنوشت و پایداری نانوذرات تا حد زیادی به گروههای عاملی پوشش سطحی ذرات بستگی دارد[۴]. بیشتر نانومواد رایج، آبگریز و نامحلول هستند و تمایل به تجمع در اشکال تودهای ورسوب در سامانههای زیستی دارند. این نانوذرات درصورت ناپایداری با نشت یونهای فلزی یا رادیکالهای آزاد سمیت ایجاد میکنند. پوششهای خاص نانوذرات اعم از سورفکتانت، پلیمر و انواع گروههای عاملی[۳]، با افزایش پایداری و انحلالپذیری ذرات در مایعات بیولوژیک، سمیت نانوذرات را میتوانند کاهش داده و باعث تعامل نانوذرات با سلولهای انتخابی شوند[۵]. در آزمایشی بر ماهی مدیکا، اثر سمیت نانوذرات تکلایهی طلا با پوشش عاملهای آبدوست و آبگریز بررسی شد. براساس نتایج به دست آمده، ذرات آبگریز در تمامی اعضای بدن پراکنده شده و باعث مرگ ماهی در کمتر از ۲۴ساعت شدند. درحالیکه ذرات آبدوست هیچ اثر واضحی بر سلامتی ماهی نداشتند[۱].
انواع پوششهای سطحی زیستسازگار، باعث بهبود خواص زیستی نانوسامانههای هدفمند انتقال دارو میشوند. برای مثال از نانوذرات اکسیدآهن به دلیل قابلیت کنترل از طریق میدان مغناطیسی خارجی، به صورت گسترده در تصویربرداری تشدید مغناطیسی[۲] استفاده میشود. نانوذرات اکسید آهن با پوشش پلیمرهای پرشاخه گلیسرول، با داشتن تعداد زیادی از گروههای عاملی، به صورت بهینه و هدفمند دارورسانی میکنند. در آزمون سمیت سلولی، بررسیهای مربوط به زیستسازگاری نانوذرات اکسید آهن نشان داد که نمونههای بدون پوشش از غلظت μg/ml ۲۰۰ به بالا، سمیت سلولی داشتند، درحالیکه نمونههای پوششدار فاقد این اثر سمیت بودند[۱۱]. در جدول۲، چگونگی تغییر الگوهای تجمع و توزیع نانوذرات دارویی در بدن با انواع پوششهای سطحی نشان داده شدهاست.
جدول۲- اثر پوشش سطحی نانوذرات دارویی در سرنوشت، کاربرد و توزیع در بدن[۴]
|
پوشش |
اثر |
کاربرد |
|
بدون پوشش |
برداشت توسط ماکروفاژ |
MRI |
|
IgG |
برداشت توسط سلولهای ایمنی |
ردیابی سلولهای ایمنی |
|
PEG |
بهبود زمان باقی ماندن در گردش خون |
دارورسانی |
|
فولات |
هدفمند کردن اختصاصی ذرات برای بافت تومور |
دارورسانی |
۳-جمعبندی و نتیجه گیری
نانوذرات در کنار بسیاری از کاربردهای صنعتی و پزشکی، دارای برخی ویژگیهای سمی در برهمکنش با سلولهای زنده هستند. فعالیتهای طبیعی و انسانی باعث رهایش مقدار زیادی از انواع نانوذرات در محیطزیست شده و نگرانی بزرگی در حوزه سلامت و بهداشت محیط ایجاد کرده است. مطالعات سمشناسی در ابعاد نانو، به رابطهی خواص فیزیکوشیمایی، از قبیل ترکیب شیمیایی، اندازه و توپوگرافی سطح با میزان واکنش نانوذرات با سلولهای زنده میپردازد. مواد نمکی موجود در سرم، با تغییرات الکترواستاتیک در بار نانوذرات، پایداری و سرنوشت برهمکنش ذرات با سلولها را تحت تاثیر قرار میدهد. بنابراین، مشخصهیابی نانوذرات نه تنها در محیط خشک، بلکه در تمام محیطهای فیزیولوژیک مانند سرم و مایعات بدن(پایداری کلوئیدی، پتانسیل سطح، قطر هیدرودینامیک) حائز اهمیت است.
مطالعات فردی در زمینه سمشناسی نیازمند استانداردسازی آزمونها و شرایط آزمایشگاهی است. در نظر گرفتن غلظت به عنوان یک پارامتر مهم در سمیت و بررسی اثرات طولانی مدت نانوذرات در هموستاز و حیات سلولها، تجمع و پایداری نانوذرات در داخل سلول پس از چندین روز و هفته، چالش بزرگی در این زمینه است. با این حال مطالعات سمیت شناسی با وجود مشکلات ارزیابی سمیت و سنجش غلظت نانوذرات، در حال گسترش است. روشهای مناسبی در استانداردهای راهنمایی و آئیننامههای کار، به منظور جلوگیری از مواجهه با خطرات نانومواد، کاهش اثرات زیستمحیطی، تامین سلامت و ایمنی کارکنان منتشر شدهاست. در مقالات بعدی با بیشتر جزئیات آنها آشنا میشویم.
۴- مراجع
[۱]فرشید سلیمانی، ایرج نبی پور، فاطمه فرجی، سینا دوبرادران، اثرات نانوذرات بر انسان و محیط زیست : مروری بر سمیت، مواجهه، راههای کنترل خطرات و چشماندازهای آینده، طب جنوب، شماره سوم، سال۹۴، صفحه ۶۳۰-۶۶۳
[۲] معصومه تاران، قاسم عموعابدینی،فائزه کاشانیان، بررسی سمیت نانوذرات در مواجهه با سلول، ایمنی زیستی، شماره اول، سال ۹۲، صفحه های ۵۵ تا ۷۰
[۳] عمید رهی، نغمه ستاراحمدی، حسین هلی، سمیت نانو مواد- تاثیر خواص فیزیکوشیمیایی، دانشگاه علوم پزشکی شهید صدوقی یزد، شماره ۶، سال۹۳، صفحه های ۱۷۳۷-۱۷۵۴
[۴]حسین قنبری، سازگاری زیستی در مقیاس نانو، اول، تعالی اندیشه، سال۱۳۹۴.
[5] Sukhanova, Alyona, et al. "Dependence of nanoparticle toxicity on their physical and chemical properties." Nanoscale research letters 13.1 (2018): 44.
[6]Bahadar, Haji, et al. "Toxicity of nanoparticles and an overview of current experimental models." Iranian biomedical journal20.1 (2016): 1.
[7]Sun, Xin-Yuan, Qiong-ZhiGan, and Jian-Ming Ouyang. "Size-dependent cellular uptake mechanism and cytotoxicity toward calcium oxalate on Vero cells." Scientific reports 7 (2017): 41949.
[8]Huang, Yue-Wern, Melissa Cambre, and Han-Jung Lee. "The toxicity of nanoparticles depends on multiple molecular and physicochemical mechanisms." International journal of molecular sciences 18.12 (2017): 2702.
[9]Zhang, Bokai, et al. "Shape dependent cytotoxicity of PLGA-PEG nanoparticles on human cells." Scientific reports 7.1 (2017): 7315.
[10]Geng, Y. A. N., et al. "Shape effects of filaments versus spherical particles in flow and drug delivery." Nature nanotechnology 2.4 (2007): 249.
[۱۱] عاطفه زارعپور، محمد رفیعینیا، علی ضرابی،حسین صالحی،طراحی، ساخت، مشخصهیابی و ارزیابی زیستی نانوذرات اکسید آهن پوشش داده شده با پلیمر پرشاخه پلیگلیسرول، پژوهشهای سلولی و مولکولی، شماره اول، سال ۹۵، صفحه های ۸۰ تا ۹۱
۵- پاورقیها
[1]In-vivo
[2]Magnetic resonance imaging (MRI)