چهارشنبه 17 دی 1399 کد خبر: 75

۱-مقدمه
حدود دوسوم سطح زمین را آب پوشش میدهد. با این وجود، سالهاست بشر با معضل کمبود آب پاکیزه روبرو است. طبیعت به طور خودکار آب را تصفیه کرده و آب پاکیزه را در اختیار انسان قرار میدهد؛ اما رشد بی وقفه جمعیت و گسترش صنایع، منجربه مختلشدن چرخه طبیعی تصفیه آب شده که کمبود آب پاکیزه در دسترس را به دنبال داشته است. حدود ۹۰ درصد بیماریهای کشورهای درحال توسعه، بر اثر آبهای آلوده ایجاد میشوند[۱]. بنابراین تصفیه پساب به منظور حفظ محیطزیست و سلامت انسان، موضوع بسیار مهمی است. روشهای سنتی تصفیه پساب، نیاز به سرمایهگذاری کلان، انرژی زیاد و زیرساخت وسیع دارد. به همین دلیل پیدا کردن فناوریهای ارزان و با بازده بالا از اهمیت ویژهای برخوردار است. فناورینانو، راهکارهای موثری برای حل این چالشها پیشنهاد میدهد. این فناوری شامل استفاده از مواد در ابعاد نانومتر برای حل مشکلات میشود. نانومواد انرژی سطحی بالا، سطح ویژه زیاد و خواص وابسته به سطح دارند. در این مقاله به بررسی انواع پساب، روشهای سنتی تصفیه پساب و تصفیه پساب با استفاده از فوتوکاتالیستها خواهیم پرداخت.
۲-پسابها و روشهای تصفیه آنها
۱-۲- انواع پسابها و ترکیبات آنها
پسابها را میتوان به دودسته تقسیم کرد؛ پسابهای خانگی و پسابهای صنعتی. پسابهای خانگی که با عنوان فاضلاب شهری نیز شناخته میشوند، رقیقتر از پسابهای صنعتی بوده و بیش از ۹۹ درصد آن را آب تشکیل میدهد و مابقی آن شامل جامدات معلق، ترکیبات آلی زیست تخریبپذیر، جامدات معدنی، ترکیبات مغذی، فلزات و میکروارگانیسمهای پاتوژنیک[۱] میباشند[۲]. ترکیبات آلی زیست تخریبپذیر متشکل از مواد کربنی مانند پروتئینها، کربوهیدراتها و چربیها میباشد که قابلیت تبدیل به کربن دیاکسید را دارند. فاضلاب شهری همچنین شامل مواد مغذی مانند نیتروژن و فسفر است که برای جلوگیری از ایجاد سمیت در محیط زیست لازم است تصفیه شوند.
پسابهای صنعتی محصول شرکتها، مزارع کشاورزی و فعالیتهای عمومی (بیمارستانها، فروشگاهها، رستورانها و...) است. ترکیبات پسابهای صنعتی وابسته به منبعی است که پساب از آن حاصل میشود. برای مثال پساب صنایع نساجی، بیشتر شامل رنگهای آلی میشود در حالیکه پساب رستورانها عمدتا شامل چربیها است. بعلاوه، پسابی که از صنایع مختلف و زمینهای کشاورزی به وجود میآید، شامل مقادیر زیاد مواد شیمیایی مضر و آلایندههای آلی است. یونهای فلزات سنگین یکی دیگر از مواد درون پسابهای صنعتی هستند که برای ارگانیسمهای زنده، سمی درنظر گرفته میشوند.
۲-۲- تصفیه پساب
تصفیه پساب، فرایندی است که در آن آلایندهها پیش از آنکه وارد محیطزیست شوند، با استفاده از پروسههای فیزیکی یا شیمیایی از فاز آبی جدا میشوند. روشهای زیادی برای تصفیه پسابهای خانگی و صنعتی وجود دارد. متداولترین روش آن، تصفیهخانههای شهری هستند که درصورت استفاده بهینه میتوانند بخش زیادی از آلایندهها را از آب حذف کنند. این روش تصفیه از سه مرحله پیشین، اولیه و ثانویه تشکیل میشود[۲].
مرحله پیشین شامل حذف تکههای بزرگ یا سنگین از فاضلاب میشود. مراحل غربال و حذف ریگ و ماسه در این مرحله انجام میشود. در فرایند غربالگری، تکههای بزرگ شناور مانند سنگ، کاغذ و پلاستیک با استفاده از صافیها جدا میشوند. مواد جدا شده توسط صافیها، معمولا دفن یا سوزانده میشوند. حذف شن و ماسه مرحله بعدی پس از غربالگری است که از طریق تهنشینی انجام میشود.
پس از عبور از مرحله پیشین، پساب باقیمانده وارد مرحله اولیه میشود. این مرحله شامل جدا کردن بخش زیادی از جامدات معلق در پساب به روش رسوبگذاری است. پساب وارد تانکرهای رسوبگذاری میشود؛ جایی که زمان کافی برای ته نشینی جامدات(لجن) وجود دارد. پساب چند ساعت درون تانکر باقی میماند تا لجنها تهنشین شده و لایهای از کف روی سطح پساب ایجاد شود. سپس کف از بالا سرریز و لجن از پایین جدا میشوند و پساب وارد مرحله ثانویه میشود. در مرحله تصفیه اولیه، تا ۴۰% اکسیژن مورد نیاز بیولوژیکی ()[۲] کاهش مییابد. (BOD فاضلاب در واقع میزان اکسیژن مورد نیاز فاضلاب است تا میکروارگانیسمها بتوانند مواد آلی موجود در آن را اکسید نمایند. کاهش این مقدار به معنای کاهش میزان اکسیژن مورد نیاز برای تصفیه پساب و در نتیجه از بین رفتن برخی آلایندههای آلی میباشد.) همچنین در این مرحله ۸۰% تا ۹۰% جامدات معلق از پساب حذف میشوند. با وجود این که تصفیه اولیه مقدار زیادی از آلایندههای موجود در پساب را از بین میبرد، اطمینان کافی برای حذف تمام آلاینده های مضر را نمیدهد.
پساب باقیمانده از مرحله اولیه حاوی مقدار قابل توجهی آلایندههای آلی و اندکی جامدات معلق است. برای حذف آلایندههای باقیمانده، پساب وارد مرحله تصفیه ثانویه میشود. این مرحله شامل فرایندهای بیولوژیکی است که میتواند سطح BOD پساب را کاهش داده و همچنین مقدار کمی از فلزات معلق را نیز حذف نماید. در این مرحله، به منظور رشد باکتریهای هوازی و سایر میکروارگانیسمهایی که آلایندههای آلی را به آب و کربن دیاکسید تجزیه میکنند، پساب تحت هوادهی شدید قرار میگیرد. علاوه بر حذف آلایندههای آلی، برخی مواد مغذی مانند نیتروژن و فسفر نیز در این مرحله حذف میشوند. شکل ۱ نمایی از فرایند کامل تصفیه خانه که شامل سه مرحله است را نشان میدهد.
پس از اینکه مراحل تصفیه پساب انجام شد، باید توجه داشت که آب باقیمانده برای ورود به محیط زیست به اندازه کافی پاک باشد. بعلاوه لجن به دست آمده در فرایند تصفیه حاوی آلایندههای مضر فراوانی است؛ از این رو کنترل کردن لجن باقیمانده از اهمیت به سزایی برخوردار است. معمولا پیش از دفع پساب به محیط زیست، فرایندهای کلریناسیون[۳] یا ضدعفونیسازی با استفاده از تابشفرابنفش[۴] بر روی آنها انجام میشود. بر روی لجن نیز فرایندی غیرهوازی انجام میشود که در آن باکتریهای بیهوازی در لجن رشد میکنند. این باکتریهای بیهوازی با تجزیه جامدات آلی موجود در لجن به محصولات جانبی قابل انحلال در آب یا گازها (غالبا متان و کربن دیاکسید)، میزان این جامدات آلی در لجن را کاهش میدهند. گاز متان تولید شده در این فرایند میتواند بعنوان سوخت در سایر بخشهای تصفیه خانه مورد استفاده قرار بگیرد. سپس لجن باقیمانده برای پرکردن زمین به کار برده میشود.
پس از این مراحل متداول، برخی تصفیه خانهها مرحله سوم تصفیه پساب را نیز به فرایند گندزدایی اضافه میکنند که در آن آلایندههای آلی و معدنی باقیمانده و همچنین میکروارگانیسمهایی که از مرحله ثانویه باقیماندهاند توسط روشهای فیزیکی و شیمیایی حذف میشوند [۳]. پساب پس از گذشتن از مرحله سوم تصفیه به استانداردهای مورد نظر برای آب آشامیدنی خواهد رسید. با این وجود، این مرحله بسیار هزینه بر است و به ندرت توسط صنایع مورد استفاده قرار میگیرد.

شکل۱- نمایی از فرایند تصفیه پساب در تصفیه خانه [۲]
۳- استفاده از فناوری نانو برای تصفیه پساب
علوم و فناوری نانو به مطالعه مواد در ابعاد نانومتر میپردازد. در این ابعاد، مواد ویژگیها و خواص جالب توجهی از خود نشان میدهند. علت بروز این خواص، اندازه کوچک این ذرات است. فناوری نانو بر اساس دستکاری، کنترل و ترکیب اتمها و مولکولها به منظور رسیدن به مواد، ترکیبات و ساختارهایی است که در ابعاد نانومتر باشند. در سالهای اخیر، توسعه ابزارها و روشهایی که مبتنی بر فناوری نانو بودهاند، کمک شایانی به حل معضلات موجود در زمینه تصفیه پساب کردهاند[۴و۵]. علت اهمیت این روشها، کوچک بودن نانوذرات، واکنشپذیری بالای آنها و قابلیت تولید آنها با استفاده از روشهای دوستدار محیطزیست میباشد. مهمترین روشهای کارآمد برای تصفیه پساب بدین شرح میباشند:
در این مقاله فرایندهای فوتوکاتالیستی مورد برسی قرار میگیرند و دو روش دیگر در مقاله بعدی بررسی خواهند شد.
۴- فرایندهای فوتوکاتالیستی
استفاده از فوتوکاتالیستها روشی کارآمد برای تصفیه پساب است که در آن از نانوساختارهای کاتالیست استفاده میشود که با تابش نور فعال میشوند و قادر به حذف آلایندههای مختلفی هستند که در آب وجود دارد. تعریف فرایند فوتوکاتالیز بدین شرح است: تغییرات در نرخ انجام یک واکنش شیمیایی یا شروع آن واکنش که در اثر تابش فرابنفش، مرئی یا فروسرخ در حضورمادهای به نام "فوتوکاتالیست" که نور را جذب کرده و در تغییرات شیمیایی ایجاد شده شرکت میکند[۶]. در فرایند معمول فوتوکاتالیست، یک ماده نیمهرسانا بعنوان کاتالیست مورد استفاده قرار میگیرد که در معرض نور قرار گرفته تا با جذب انرژی نور که لازم است برابر یا بیشتر از گاف انرژی[۸] آن باشد، زوج الکترون- حفره[۹] (اکسایتون) را تولید کند. زوج الکترون حفره حاصل، قادر هستند رادیکالهای فعال اکسنده یا کاهنده مانند سوپراکسید و یون هیدروکسیل را در آب تولید نمایند. سپس این رادیکالها از طریق یک سری واکنش ثانویه، آلایندههای آلی و معدنی موجود در پساب را حذف میکنند. حذف آلایندههای موجود در آب همچنین از طریق انتقال مستقیم الکترونها یا حفرههایی که توسط نور تولید شدهاند، از سطح کاتالیست به مولکولهای آلاینده نیز ممکن است. شکل۲ نمایی از فرایند فوتوکاتالیستی که در سطح نانوساختارهای نیمههادی اتفاق میافتد را نشان میدهد.
فرایند فوتوکاتالیستی فرایندی است که مکانیزم کلی آن پیچیده بوده و از پنج مرحله اصلی تشکیل شده است[۷]:
مجموعه واکنشهای فوتوکاتالیستی ممکن برای تجزیه و حذف آلایندهها در ادامه آمده است[۸].
به دنبال تولید گونههای رادیکالی، آلایندهها با آنها واکنش داده و کربن دیاکسید، اسیدهای معدنی و فراوردههای هیدروکسیلاته تولید میکنند. شکل۲ شماتیکی از فرایند تصفیه فوتوکاتالیستی را نشان میدهد[۸].
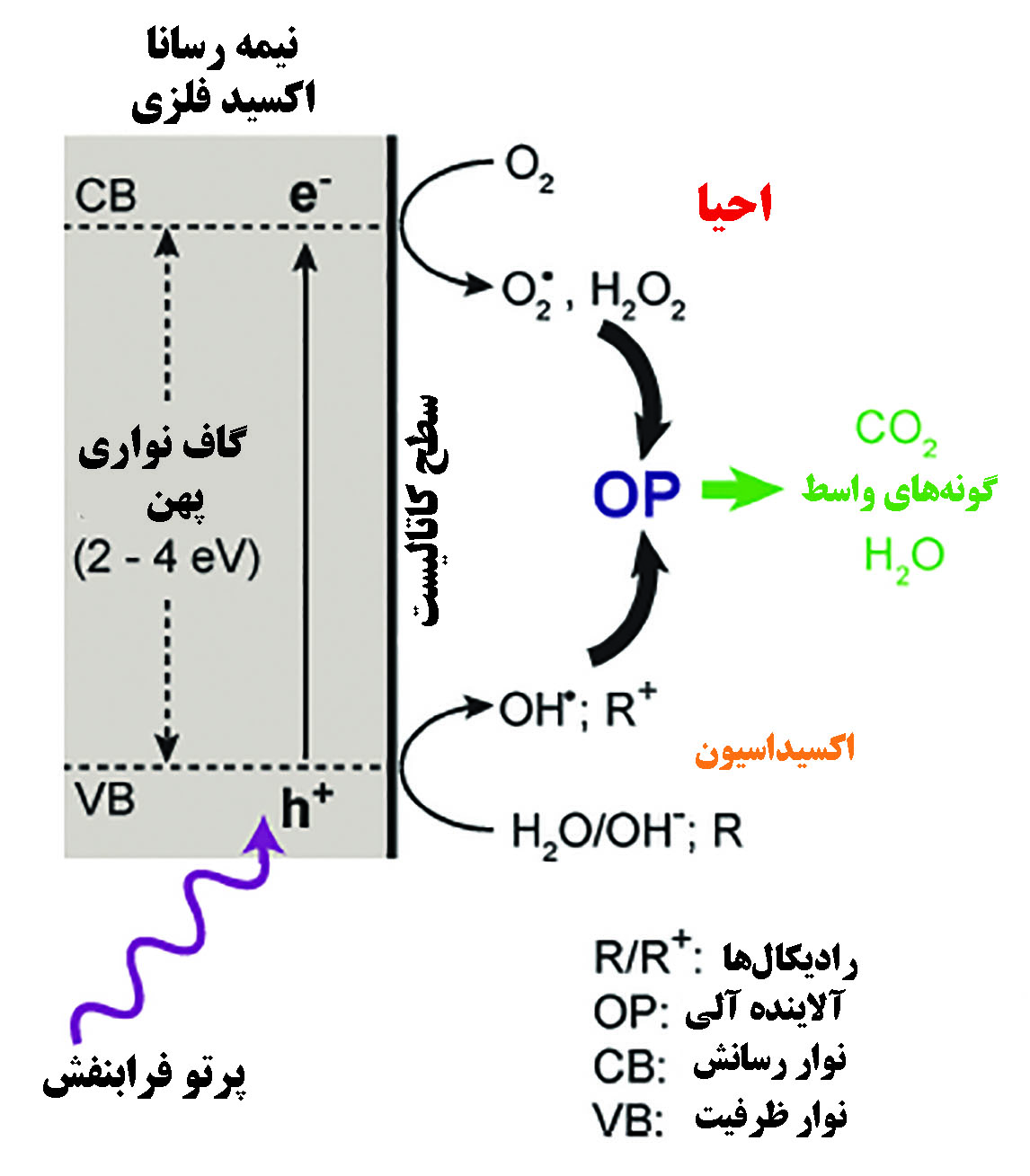
شکل۲- فرایند تصفیه فوتوکاتالیستی[۸]
فعالیت فوتوکاتالیستی شدیدا وابسته به توانایی فوتوکاتالیست در تولید زوج الکترون- حفره با دریافت نور است. اکسایتونهای تولید شده ناپایدار هستند و عمر آنها کوتاه است و پایدارسازی آنها برای واکنشهای ثانویه ضروری میباشد.
کاربرد نیمهرساناهای نانوساختار در فرایندهای فوتوکاتالیستی بیشتر از نیمهرساناهای بالک است؛ زیرا سطح ویژه زیاد نانوذرات قابلیت تجمع الکترونها و حفرهها روی سطح را فراهم میآورد. برای یک فوتوکاتالیست کارآمد، نیمهرسانا باید گاف نواری بزرگی داشته باشد تا بتواند انرژی کافی برای انجام واکنشهای ثانویه را فراهم کند و همچنین بازترکیب اکسایتون به حداقل برسد. یک فوتوکاتالیست ایدهآل باید خواص زیر را داشته باشد[۹]:
متداولترین فوتوکاتالیستهای نانوساختار مورد استفاده عبارتند از تیتانیوم دیاکسید، اکسید روی، فریک اکسید، سولفید روی و سولفید کادمیوم[۱۰].
نیمهرساناهایی که گاف نواری بزرگ دارند، نور را در محدوده فرابنفش جذب میکنند؛ در حالیکه استفاده از نور پر انرژی فرابنفش برای برانگیخته کردن اکسایتونها صرفه اقتصادی ندارد. از این رو تحقیقات زیادی بر روی استفاده از نور مرئی برای این فوتوکاتالیستها انجام شده است. نور خورشید که به سطح زمین میرسد از ۴۶ درصد نور مرئی، ۴۷ درصد تابش فروسرخ و تنها ۷ درصد نور فرابنفش تشکیل شده است. برای استفاده از نور خورشید جهت برانگیختن الکترون در فوتوکاتالیستهای با گاف نواری بزرگ روشهای زیر پیشنهاد شدهاند

شکل۳- گاف نواری کوپل اکسید روی – اکسید مس که نیتروژن در آنها دوپ شده است.[۲۹]
دوپ کردن به معنای وارد کردن عناصر مهمان در ساختار کریستالی میزبان به عنوان یک نقص بلوری است که میتواند ساختار نواری ماده را دچار تغییر کند. در شکل۳ شماتیک گاف نواری کوپل اکسیدروی- اکسید مس که نیتروژن در آنها دوپ شده است نشان داده شده است[۲۹].
۱-۴- حذف آلایندههای آلی
فرایند فوتوکاتالیستی برای تصفیه آلایندههای آلی خطرناک به مواد بی خطری مانند کربن دیاکسید و آب استفاده فراوانی دارد. با استفاده از این تکنیک تصفیه، انواع مختلفی از الکلها، کربوکیسلیک اسیدها، مشتقات فنولی و ترکیبات آروماتیک کلردار حذف میشوند. انتشار رنگهای آلی ناشی از صنایع نساجی به رودخانهها تبدیل به یکی از مهمترین نگرانیها در کشورهای درحال توسعه شده است. برای تصفیه این آلایندهها از نانوذرات نیمهرسانا تیتانیوم دیاکسید و اکسیدروی استفاده میشود[۱۶].
۲-۴- حذف آلایندههای معدنی
با استفاده از واکنش فوتوکاتالیستی، آلایندههای معدنی شامل یونهای هالید، سیانید، تیوسیانات، آمونیاک، نیتراتها و نیتریدها را میتوان به خوبی از آب حذف کرد[۱۷]. طی پژوهشهای انجام شده نانوذرات تیتانیوم دیاکسید توانستهاند آلایندههای نیترات نقره[۱۸] و جیوه(II)کلرید [۱۹] را با فرایند فوتوکاتالیستی از آب حذف کنند. همچنین نانوذرات اکسیدروی با نور مرئی توانستهاند آلایندههای پتاسیم سیانید[۲۰] و کروم شش ظرفیتی[۲۱] را تصفیه کنند. در پژوهشی با استفاده از کامپوزیت نانولوله کادمیوم سولفید/ تیتانات اکسیداسیون فوتوکاتالیستی آمونیاک در آب مشاهده شده است[۲۲].
۳-۴- حذف فلزات سنگین
حذف فلزات سنگین از پساب، یکی دیگر از چالشهای موجود در تصفیهخانهها میباشد؛ زیرا مقدار آن در پساب با توجه به نوع پساب میتواند متغیر باشد. برای حفظ سلامت انسان و افزایش کیفیت آب، حذف این آلایندهها از پساب اهمیت ویژهای دارد. با این وجود، با توجه به کمیاب بودن و ارزش بالای برخی از این فلزات، بازیابی آنها نسبت به حذف آنها ترجیح داده میشود. با استفاده از فرایند فوتوکاتالیستی، فلزات سنگین متنوعی قابل بازیابی هستند[۲۳]. بازیابی طلای سه ظرفیتی، پلاتین چهارظرفیتی و رودیوم سه ظرفیتی با استفاده از نانوذرات تیتانیوم دیاکسید نشان داده شده است؛ در این پژوهش ۹۰ درصد طلا در pH صفر تحت تابش مرئی بازیابی شدند[۲۴].در پژوهشی دیگر با استفاده از نانوذرات تیتانیوم دیاکسید، کادمیوم از پساب حذف شد. در این پژوهش با استفاده از تابش نور با طولموج ۲۵۳/۷ نانومتر، بیش از ۹۰ درصد کادمیوم موجود در پساب حذف شده و روی سطح نانوذرات تیتانیوم دیاکسید جذب شدند[۲۵]. به منظور بازیابی فلز جیوه از پساب حاوی یونهای این فلز، گروهی از محققان از کربن فعال و نانوذرات تیتانیوم دیاکسید استفادهکردند. با تلفیق این دو ماده، پس از تابش نور و انجام فرایند فوتوکاتالیستی، ۷۰ درصد جیوه موجود در پساب بر روی کربن فعال و نانوذرات تیتانیوم دیاکسید بازیابی شدند[۲۶]. در پژوهشی فرایند حذف کروم شش ظرفیتی با استفاده از نانوکامپوزیت تیتانیوم دی اکسید/ طلا بررسی شده و با تیتانیوم دیاکسید به تنهایی مقایسه شده است. تحت تابش نور فرابنفش، کامپوزیت ۹۱ درصد حذف کروم و نانوذرات تیتانیوم دیاکسید ۸۷ درصد حذف کروم را نشان دادند. علت موثرتر بودن حذف با استفاده از کامپوزیت، جذب نور در محدوده وسیعتر به دلیل پدیده پلاسمون سطحی است که در نانوذرات طلا اتفاق میافتد بعلاوه کاهش آهنگ بازترکیب زوج اکسایتون به دلیل حضور نانوذرات طلا[۲۷].
۴-۴- حذف میکروبها
اکثر فوتوکاتالیستها اثر ضدمیکروبی نیز از خود نشان میدهند و در برابر رشد میکروارگانیسمها مقاومت میکنند. فرایند حذف میکروبها اساسا شامل تخریب دیواره سلولی با استفاده از رادیکالهای فعالی است که طی واکنشهای فوتوکاتالیستی تولید میشوند؛ که درنهایت منجر به تخریب میکروب میشود. باکتریهای متنوعی مانند اشرشیا کلای (گرم منفی) و استافیلوکوکوس اورئوس(گرم مثبت) را میتوان با استفاده از فرایند فوتوکاتالیستی از پساب حذف کرد[۲۸].
۵- جمعبندی و نتیجهگیری
تصفیه پساب، فرایندی است که در آن آلایندهها با استفاده از فرایندهای فیزیکی یا شیمیایی از فاز آبی جدا میشوند. پسابهای شهری عمدتا از آب تشکیل شدهاند اما پسابهای صنعتی بسته به منبع آنها میتوانند غنی از رنگهای آلی، چربیها، فلزات و... باشند. تصفیهخانهها معمولا پساب را در سه مرحله پاکسازی میکنند. اما این مراحل قادر به جداسازی تمام آلایندهها مانند رنگهای آلی و فلزات سنگین نمیباشند. بعلاوه اینکه هزینه تمام شده این نوع از تصفیه به دلیل احتیاج به زیرساخت فراوان زیاد است. نانوذرات به دلیل سطح ویژه بالا و همچنین واکنشپذیری زیاد، میتوانند در فرایندهای تصفیه پساب مورد استفاده قرار گیرند. فوتوکاتالیستها دستهای نانوذرات هستند که با دریافت تابش، در صورتی که انرژی تابش بیشتر یا برابر با گاف نواری آنها باشد، زوج الکترون-حفره(اکسایتون) تولید میکنند. اکسایتونهای تولیدی در محیط مرطوب توانایی تولید رادیکالهای هیدروکسیل دارند که این رادیکالها میتوانند آلایندهها را اکسید کرده و آنها را از پساب حذف کنند. با استفاه از فوتوکاتالیستها میتوان آلایندههای آلی، معدنی، فلزات سنگین و میکروبها را از پساب حذف کرد.
۶- منابع
[1] C. Fishman, The Big Thirst: The Secret Life and Turbulent Future of Water, Free Press, New York (2011).
[2] M. R. Templeton and P. D. Butler, Introduction to Wastewater Treatment, Bookboon, London (2011)
[3] G. Tchobanoglous, F. L. Burton, and H. D. Stensel, Wastewater Engineering: Treatment and Reuse, McGraw-Hill Education, Whitby, Canada (2003).
[4] Baruah, Sunandan, and Samir K. Pal and Joydeep Dutta. “Nanostructured Zinc Oxide for Water Treatment.” Nanoscience& Nanotechnology-Asia, vol. 2, no. 2, 2012, pp. 90–102, doi:http://dx.doi.org/10.2174/2210681211202020090.
[5] Baruah, Sunandan, and Joydeep Dutta. “Hydrothermal Growth of ZnO Nanostructures.” Science and Technology of Advanced Materials, vol. 10, no. 1, Taylor & Francis, Jan. 2009, p. 13001, doi:10.1088/1468-6996/10/1/013001.
[6] A. D. McNaught and A. Wilkinson, IUPAC Gold Book, Blackwell Scientific Publications, Oxford (1997).
[7]Pirkanniemi, Kari, and Mika Sillanpää. “Heterogeneous Water Phase Catalysis as an Environmental Application: A Review.” Chemosphere, vol. 48, no. 10, 2002, pp. 1047–60, doi:https://doi.org/10.1016/S0045-6535(02)00168-6.
[8] V. Pareek and A. A. Adesina, Handbook of Photochemistry and Photobiology: Inorganic Photochemistry, edited by H. S. Nalwa, American Scientific Publishers, Los Angeles (2003).
[9] Bhatkhande, Dhananjay S., et al. “Photocatalytic Degradation for Environmental Applications – a Review.” Journal of Chemical Technology & Biotechnology, vol. 77, no. 1, John Wiley & Sons, Ltd, Jan. 2002, pp. 102–16, doi:10.1002/jctb.532.
[10] Hagfeldt, Anders., and Michael. Graetzel. “Light-Induced Redox Reactions in Nanocrystalline Systems.” Chemical Reviews, vol. 95, no. 1, American Chemical Society, Jan. 1995, pp. 49–68, doi:10.1021/cr00033a003.
[11] KG, Kanade, et al. “Self-assembled aligned Cu doped ZnO nanoparticles for photocatalytic hydrogen production under visible light irradiation.” Materials Chemistry and Physics, vol. 102, no. 1, 2007, pp. 98–104, doi:10.1016/j.matchemphys.2006.11.012.
[12] Graciani, Jesús, et al. “A Theoretical Insight into the Catalytic Effect of a Mixed-Metal Oxide at the Nanometer Level: The Case of the Highly Active Metal/CeOx/TiO2(110) Catalysts.” The Journal of Chemical Physics, vol. 132, no. 10, American Institute of Physics, Mar. 2010, p. 104703, doi:10.1063/1.3337918.
[13] Wu, Ling, et al. “Characterization and Photocatalytic Mechanism of NanosizedCdS Coupled TiO2 Nanocrystals under Visible Light Irradiation.” Journal of Molecular Catalysis A: Chemical, vol. 244, no. 1, 2006, pp. 25–32, doi:https://doi.org/10.1016/j.molcata.2005.08.047.
[14] Cheng, Mingming, et al. “Photocatalytic Degradation of Organic Pollutants Catalyzed by Layered Iron(II) Bipyridine Complex–Clay Hybrid under Visible Irradiation.” Applied Catalysis B: Environmental, vol. 65, no. 3, 2006, pp. 217–26, doi:https://doi.org/10.1016/j.apcatb.2006.01.010.
[15] Kochuveedu, Saji Thomas, et al. “Surface-Plasmon-Induced Visible Light Photocatalytic Activity of TiO2 Nanospheres Decorated by Au Nanoparticles with Controlled Configuration.” The Journal of Physical Chemistry C, vol. 116, no. 3, American Chemical Society, Jan. 2012, pp. 2500–06, doi:10.1021/jp209520m.
[16] Danwittayakul, Supamas, et al. “Enhancement of Photocatalytic Degradation of Methyl Orange by Supported Zinc Oxide Nanorods/Zinc Stannate (ZnO/ZTO) on Porous Substrates.” Industrial & Engineering Chemistry Research, vol. 52, no. 38, American Chemical Society, Sept. 2013, pp. 13629–36, doi:10.1021/ie4019726.
[17] Hoffmann, Michael R., et al. “Environmental Applications of Semiconductor Photocatalysis.” Chemical Reviews, vol. 95, no. 1, American Chemical Society, Jan. 1995, pp. 69–96, doi:10.1021/cr00033a004.
[18] Ohtani, Bunsho., et al. “Photocatalytic Activity of Titania Powders Suspended in Aqueous Silver Nitrate Solution: Correlation with PH-Dependent Surface Structures.” The Journal of Physical Chemistry, vol. 91, no. 13, American Chemical Society, June 1987, pp. 3550–55, doi:10.1021/j100297a017.
[19] Serpone, N., et al. “AM1 Simulated Sunlight Photoreduction and Elimination of Hg(II) and CH3Hg(II) Chloride Salts from Aqueous Suspensions of Titanium Dioxide.” Solar Energy, vol. 39, no. 6, 1987, pp. 491–98, doi:https://doi.org/10.1016/0038-092X(87)90056-9.
[20] Doménech, J., and J. Peral. “Removal of Toxic Cyanide from Water by Heterogeneous Photocatalytic Oxidation over ZnO.” Solar Energy, vol. 41, no. 1, 1988, pp. 55–59, doi:https://doi.org/10.1016/0038-092X(88)90115-6.
[21] Yoon, Jaekyung, et al. “Photocatalytic Reduction of Hexavalent Chromium (Cr(VI)) Using Rotating TiO2 Mesh.” Korean Journal of Chemical Engineering, vol. 26, no. 5, 2009, pp. 1296–300, doi:10.1007/s11814-009-0228-1.
[22] Chen, Y. C., et al. “Photocatalytic Oxidation of Ammonia by Cadmium Sulfide/Titanate Nanotubes Synthesised by Microwave Hydrothermal Method.” Water Science and Technology, vol. 63, no. 3, Feb. 2011, pp. 550–57, doi:10.2166/wst.2011.256.
[23] Joshi, Kamlesh M., et al. "Photocatalytic removal of Ni (II) and Cu (II) by using different Semiconducting materials." Advances in Applied Science Research 2.3 (2011): 445-54.
[24] Borgarello, Enrico, et al. “Light-Induced Reduction of Rhodium(III) and Palladium(II) on Titanium Dioxide Dispersions and the Selective Photochemical Separation and Recovery of Gold(III), Platinum(IV), and Rhodium(III) in Chloride Media.” Inorganic Chemistry, vol. 25, no. 25, American Chemical Society, Dec. 1986, pp. 4499–503, doi:10.1021/ic00245a010.
[25] Skubal, L., et al. “Cadmium Removal from Water Using Thiolactic Acid-Modified Titanium Dioxide Nanoparticles.” Journal of Photochemistry and Photobiology A-Chemistry - J PHOTOCHEM PHOTOBIOL A-CHEM, vol. 148, May 2002, pp. 393–97, doi:10.1016/S1010-6030(02)00069-2.
[26] Zhang, Fu-Shen, Jerome O. Nriagu, and Hideaki Itoh. "Photocatalytic removal and recovery of mercury from water using TiO2-modified sewage sludge carbon." Journal of Photochemistry and Photobiology A: Chemistry 167.2-3 (2004): 223-228.
[27] Liu, Xinjuan, et al. “TiO2–Au Composite for Efficient UV Photocatalytic Reduction of Cr(VI).” Desalination and Water Treatment, vol. 51, no. 19–21, Taylor & Francis, May 2013, pp. 3889–95, doi:10.1080/19443994.2013.781739.
[28] Mills, Andrew, and Stephen Le Hunte. “An Overview of Semiconductor Photocatalysis.” Journal of Photochemistry and Photobiology A: Chemistry, vol. 108, no. 1, 1997, pp. 1–35, doi:https://doi.org/10.1016/S1010-6030(97)00118-4.
[29] Gaim, YohannesTeklemariam, et al. "Synthesis, Characterization and Photocatalytic Activity of N-doped Cu2O/ZnONanocomposite on Degradation of Methyl Red." Journal of Composites Science 3.4 (2019): 93.
۷- پاورقی
[1]Pathogenic micro organisms
[2]Biological Oxygen Demand (BOD)
[3]Chlorination
[4] UV disinfection process
[5]Photocatalysis
[6]Nanosorbents
[7]Nanofiltration
[8]Band gap
[9]Electron- hole pair (Exciton)
[10]Diffusion
[11] Adsorption
[12] Desorption