یکشنبه 25 خرداد 1399 کد خبر: 1
چکیده
ساختار بلوری ماده، تاثیر قابل توجهی روی خواص و ویژگیهای آن ماده دارد، از این رو مطالعه و شناخت ساختار بلوری مواد از اهمیت فراوانی برخوردار است. از آنجا که مواد جامد دارای نظم بلند برد و یا کوتاه برد هستند، به دو دسته بلوری و بیشکل[1] تقسیم میشوند. جامدات بلوری خود به دو دسته تک بلور و چند بلور تقسیم میشوند. چندبلورها دارای دانههایی هستند که در جهات مختلف رشد کردهاند و محل برخورد آنها به یکدیگر مرزدانه نام دارد. دانهبندی و مرزدانهها نقش قابل توجهی روی خواص ماده دارند. از دیگر موارد مهم در بلورشناسی، تعیین سلول واحد یک ساختار بلوری است. سلول واحد انتخابی باید به خوبی نماینده ساختار کل بلور باشد. به این منظور باید دارای ویژگیهایی باشد که در این مقاله به آنها پرداخته شده است. همچنین در این مقاله به توضیح دستهبندی جامدات، مقایسه انرژی حالت بلوری و بیشکل، انجماد مذاب فلزی و ایجاد چندبلور و تعریف شبکه/پایه در شکلدهی یک ساختار کریستالی پرداخته شده است.
کلیدواژهها: بلورشناسی، سلول واحد، تکبلور، چندبلور و بیشکل
در علم بلورشناسی، حالتهای مختلف بلوری در مواد، قوانین حاکم بر آنها، آرایشهای اتمی یا مولکولی، روشهای مشخصهیابی بلورها، خواص و ساخت بلورها مطالعه و بررسی میشود. در گذشته در بلورشناسی تمرکز بیشتر روی شکل بیرونی ساختارهای بلوری بود (مثلا در کانیشناسی)، ولی امروزه بررسیها بیشتر معطوف به ساختارداخلی بلورهاست. این تحول به ویژه پس از کشف پرتو ایکس توسط رونتگن در قرن 19 رخ داد، چراکه دانشمندان میتوانستند به کمک آن اطلاعات ارزشمندی از ساختار داخلی بلورها بدست بیاورند. به صورت کلی بلورشناسی را میتوان به عنوان شاخهای از علم که به توصیف هندسه و چینش داخلی بلورها میپردازد، تعریف نمود. در حقیقت بلورشناسی یکی از حوزههای کلیدی برای درک خواص مختلف است و با دانستن آن میتوان دلیل ویژگیهای بسیاری از مواد را توضیح داد و ساختار مواد را قبل از تولید آنها تعیین نمود [1,2].
2- دستهبندی جامدات
به صورت کلی میتوان جامدات را باتوجه به نحوه قرارگیری واحدهای سازندهشان ( این واحدها میتوانند اتمها، مولکولها و یا یونها باشند) در کنارهم، به دو دسته عمده تقسیم نمود. این دو دسته عبارتند از جامدات کریستالی و جامدات غیرکریستالی یا بیشکل. جامدات کریستالی دارای نظم بلندبرد میباشند درحالیکه جامدات بیشکل نظم کوتاهبرد دارند. این مورد در شکل1 نمایش داده شده است. همانطور که مشاهده میشود، اتمهای تشکیلدهنده در هر دو ساختار اکسیژن و سیلیسیوم هستند، اما وجود نظم با بردهای مختلف در آنها باعث ایجاد ساختارهای مختلف با خواص متفاوتی شده است. منظور از نظم کوتاهبرد در شکل1 این است که در تمام این ساختار اطراف اتم سیلیسیوم، 4 اتم اکسیژن قرار گرفتهاست. البته با توجه به اینکه شکل دو بعدی است سه اتم اکسیژن قابل مشاهده است و اتم چهارم در خارج از صفحه قرار دارد.
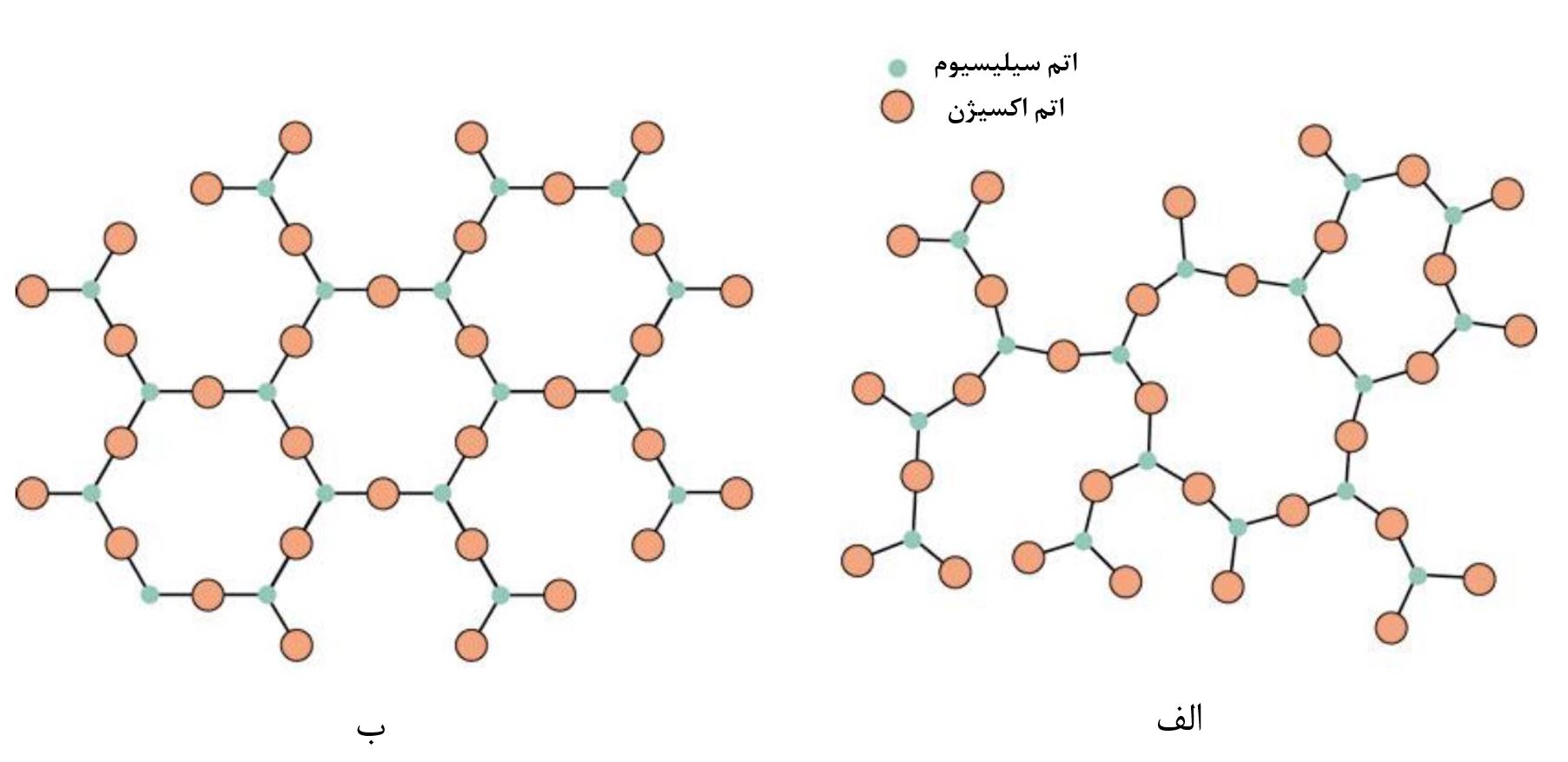
شکل1- قرارگیری اتمهای سیلیسیوم و اکسیژن در کنار هم به شکل (الف) بیشکل با نظم کوتاه برد و (ب) بلوری با نظم بلند برد [1]
قابل ذکر است که از لحاظ ترمودینامیکی مواد شیشهای (منظور موادی با ساختار بیشکل است)، شبه پایدار [2]هستند، یعنی اگر زمان و انرژی گرمایی کافی به آنها داده شود و بتوانند ساختار خود را بازچینش کنند و ساختار بلوری بیابند، سطح انرژی پایینتری را خواهند داشت. همانطور که میدانید از لحاظ ترمودینامیکی همه مواد در طبیعت تمایل دارند که سطح انرژی کمتری را داشته باشند و زمان و انرژی تعیین کننده این است که این مواد میتوانند سطح انرژی خود را کاهش بدهند و یا نمیتوانند. در شکل2 مقایسه سطح انرژی بین حالت کریستالی و بیشکل آورده شده است. مطابق این شکل مشاهده میشود که حالت بلوری سطح انرژی پایینتری نسبت به حالت بی شکل دارا میباشد [1,3].
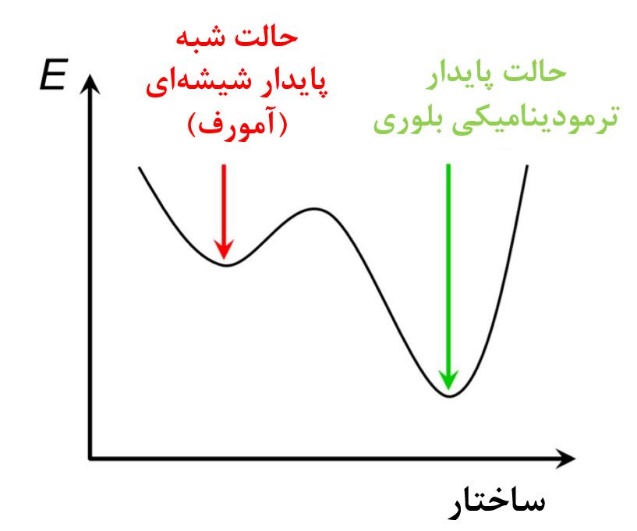
شکل2- مقایسه انرژی در حالت بیشکل و بلوری [3]
حال که مشاهده میشود ساختار بلوری سطح انرژی کمتری از بیشکل دارد پس دلیل شکلگیری ساختارهای بیشکل، چیست؟ یکی از دلایل این است که ساختار مواد تشکیلدهنده ماده پیچیده هستند (از جهت تعداد و تفاوت اندازه) و به سادگی نمیتوانند با نظمی سه بعدی و بلندبرد در کنار یکدیگر قرارگرفته و ساختار بلوری را تشکیل دهند. دلیل دیگر این است که ممکن است ساختار جامد به سرعت شکل بگیرد (مثلا یک مذاب فلزی سریع جامد شود) و اتمها یا مولکولها فرصت کافی را پیدا نکنند تا در یک ساختار بلندبرد بلوری در کنار یکدیگر قرار بگیرند [3].
قابل ذکر است که خود مواد بلوری نیز به دو دسته تقسیم میشوند که عبارتند از مواد تک بلور [3]و چندبلور[4]. در شکل3 طرحی از ساختارهای جامد تک بلور، چند بلور و بی شکل نشان داده شده است.
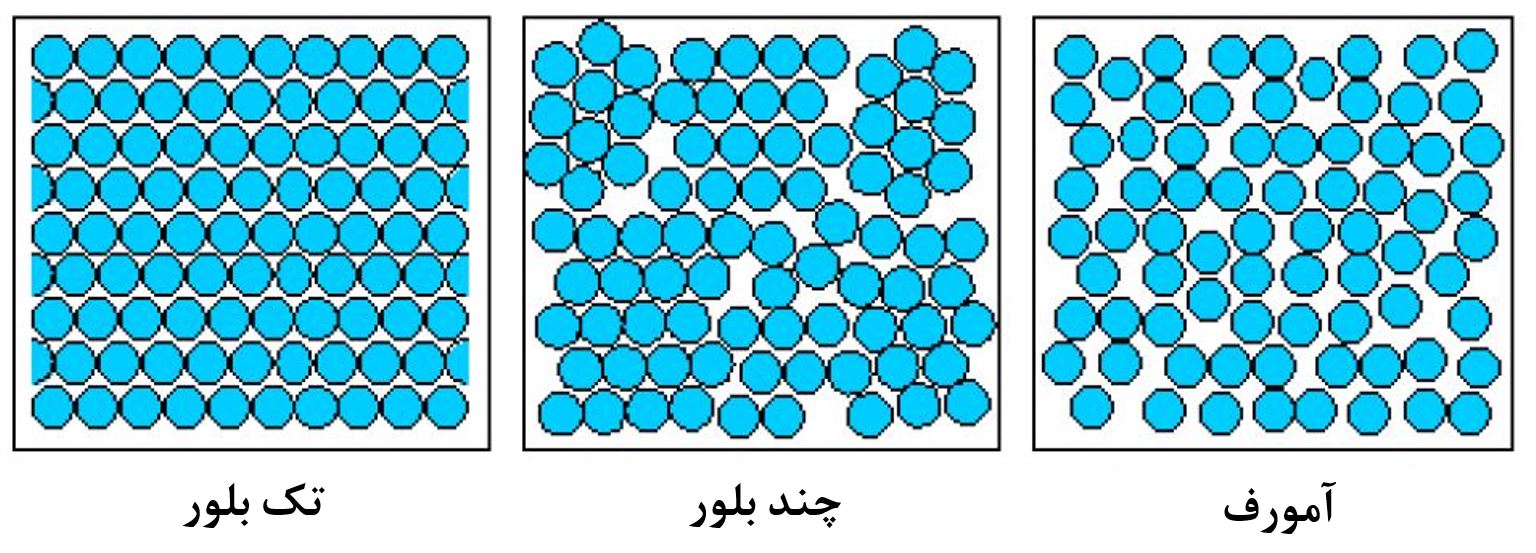
شکل3- طرحی از ساختارهای جامد تک بلور، چند بلور و بیشکل [2]
آرایش اتمها در مواد تک بلور بطور منظم، متناوب و تکرارشونده در در سراسر یک جامد بلوری است. اما مواد چندبلور دارای تعداد زیادی از بلورهای ریز (به آنها دانه گفته میشود) هستند. در هر یک از این دانهها می توانند جهتهای بلوری متفاوتی نسبت به دانههای دیگر داشته باشند. در نتیجه، یک جامد چندبلور دارای دانههای بلوری است که با یکدیگر در جهت بلوریشان تفاوت دارند. برای فهم بهتر این موضوع، بهتر است فرآیند انجماد یک مذاب فلزی را بررسی کنیم.
در حین انجماد یک مذاب فلزی، به مرور با کاهش دما، بلورهای جامد کوچکی که به آنها هسته میگوییم، در نقاط مختلف مذاب تشکیل میشوند که دارای یک نظم بلند برد هستند، ولی اندازه بسیار کوچکی دارند (شکل4-الف). با گذشت زمان و کاهش تدریجی دما، به مرور اتمهای بیشتری از مذاب به هستههای ایجاد شده میپیوندند و باعث رشد آنها در جهتهای بلوری مختلفی میشوند (شکل4-ب). در نهایت با انجماد کامل مذاب، ساختار چندبلوری به دست میآید که در آنها تفاوت جهت بلوری از دانهای به دانه دیگر وجود دارد (شکل4-ج). به مرز بین این دانهها که در واقع محل رسیدن دو دانه با جهتهای بلوری متفاوت هستند، مرزدانه گفته میشود. در شکل 4-د مرزدانهها نمایش داده شده است. همچنین در شکل4-ه تصویری واقعی از مرزدانهها در یک فلز که توسط میکروسکوپ نوری گرفته شده است، مشاهده میشود [4].
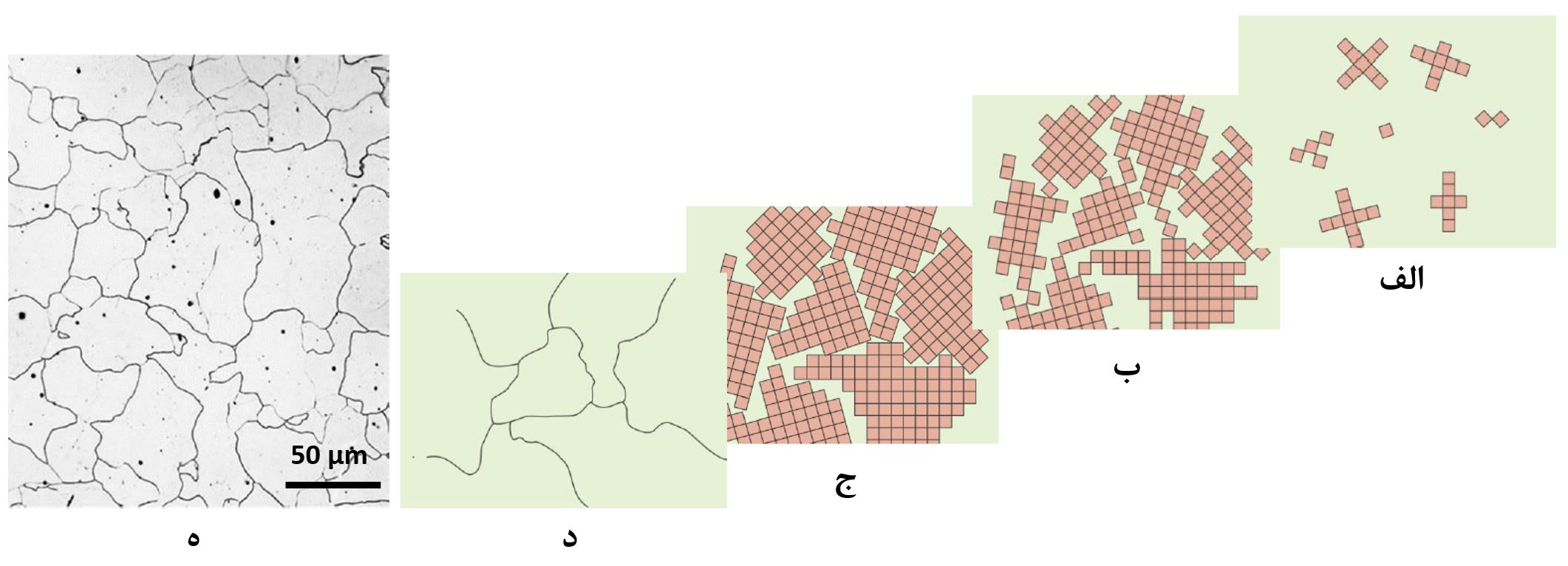
شکل4- فرآیند انجماد یک مذاب فلزی و تشکیل جامد چندبلور. الف) تشکیل هسته ب) رشد هسته ج) تکمیل رشد و انجماد کامل د) نمایش مرزدانهها به صورت شماتیک ه) تصویر میکروسکوپ نوری از دانهها و مرزدانهها [2]
در مقالات بعدی بیشتر درباره دانهها و مرزدانهها صحبت خواهد شد چراکه اهمیت فراوانی در خواص و ویژگیهای مواد بلوری دارند.
3- بلور
دو مفهوم مهم در بلورشناسی وجود دارد که عبارتند از سلول واحد [5]و شبکه [6]/ پایه [7]. نکته اساسی در تعریف سلول واحد و شبکه / پایه این است که اتمها به صورت کرههایی صلب فرض میشوند. درنتیجه مواردی همچون همپوشانی اتمها درنظر گرفته نمیشوند و اتمها مانند تیلههایی کروی و صلب درنظرگرفته میشوند.
3-1- شبکه / پایه
منظور از شبکه چینشی از نقاط در فضاست که یک مفهوم کاملا ریاضی است و منظور از پایه واحدهای ساختاری تکرارشوندهای هستند که میتوانند نقاط شبکه را اشغال کنند.
به عبارت دیگر، ساختار بلوری عبارت است از شبکهای که توسط پایهها اشغال شده است. برای فهم بهتر این موضوع به شکل 5 و 6 توجه کنید. همانطور که میبینید شبکه در واقع چینشی از نقاط است که توسط پایههای مختلفی میتواند پر شود و باتوجه به اینکه شبکه و پایه به چه صورت باشند، ساختارهای بلوری مختلفی میتواند شکل بگیرد [4].
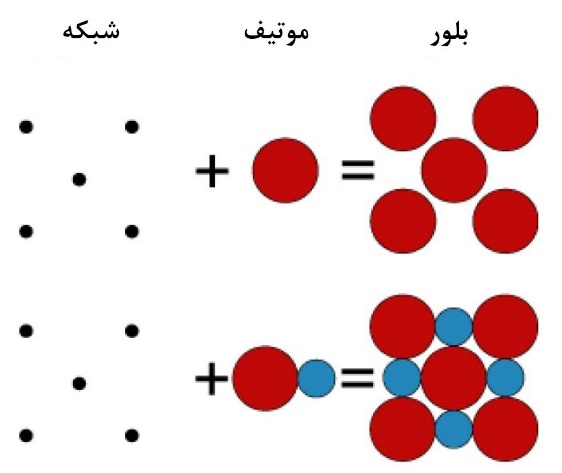
شکل5- طرحی دوبعدی از تشکیل بلور حاصل از قرارگیری پایههای گوناگون در شبکه [4]
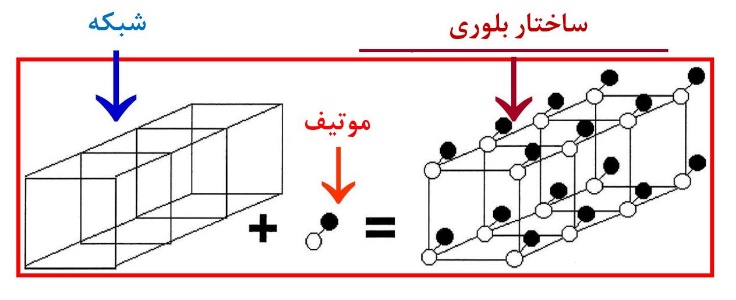
شکل6- طرحی سه بعدی از تشکیل بلور حاصل از قرارگیری پایه در شبکه [4]
همانطور که در شکل5 مشاهده میشود، پایه میتواند اتم یا گروهی از اتمها باشد که در جایگاه شبکه قرار میگیرند. در واقع شبکه به ما میگوید که تکرار آرایهها به چه صورت است، ولی پایه به ما میگوید که این آرایهها چه هستند.
3-2- سلول واحد
سلول واحد، کوچکترین واحد تکرارشونده در بلور است که با تکرار آن در سه بعد میتوان شبکه بلوری را به وجود آورد. درحقیقت، سلول واحد نماینده یک شبکه بلوری است، چراکه با دانستن آن میتوان تمام ویژگیهای هندسی بلور را دانست. برای مثال در شکل7 سلول واحد یک ساختار بلوری نمایش داده شده است. همانطور که میبینید برای ساخت این ساختار بلوری میتوان سلول واحد مشخص شده را در سه بعد تعمیم داد تا ساختار بلوری شکل7 شکل بگیرد.
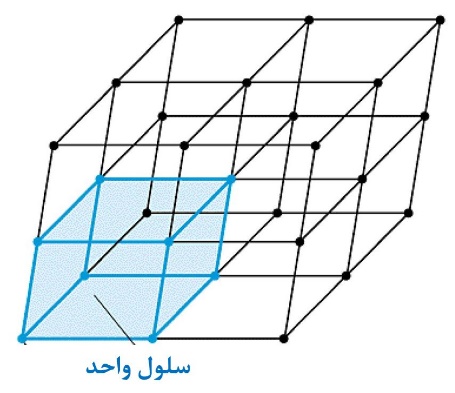
شکل7- سلول واحد در یک ساختار بلوری
برای انتخاب سلول واحد یک ساختار بلوری باید به چند نکته دقت کرد:
سلول واحد انتخابی در شکل7 دارای تمام این ویژگیها است. منظور از اینکه دارای یک نقطه شبکه باشد را با مثالی نشان میدهیم. فرض کنید شکل7 نمایش ساختار بلوری یک فلز باشد، هر کدام از نقاطی که در این شکل نشان داده شده نشانگر یکی از اتمهای آن فلز میباشد و هر اتم فلز نیز به هشت سلول واحد که در مجاورت یکدیگر قرار دارند تعلق دارد، (برای تصور این موضوع اتمی که در مرکز شکل 7 است را در نظر بگیرید، این اتم به 4 سلول واحد موجود در صفحه پایینی و 4 سلول واحد موجود در صفحه بالایی تعلق دارد). با توجه به اینکه هر اتم در هشت سلول واحد قرار دارد میتوان گفت که یک هشتم هر اتم به صورت خالص متعلق به یک سلول واحد است. از آنجا که سلول واحد نمایش داده شده دارای هشت اتم است (که یک هشتم هر کدام از آنها متعلق به آن سلول واحد است) پس داریم: 8× 18=1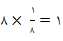 و در نتیجه یک اتم به صورت خالص متعلق به سلول واحد است که همان معنای شرط چهارم در بالا است [3,4].
و در نتیجه یک اتم به صورت خالص متعلق به سلول واحد است که همان معنای شرط چهارم در بالا است [3,4].
تمرین
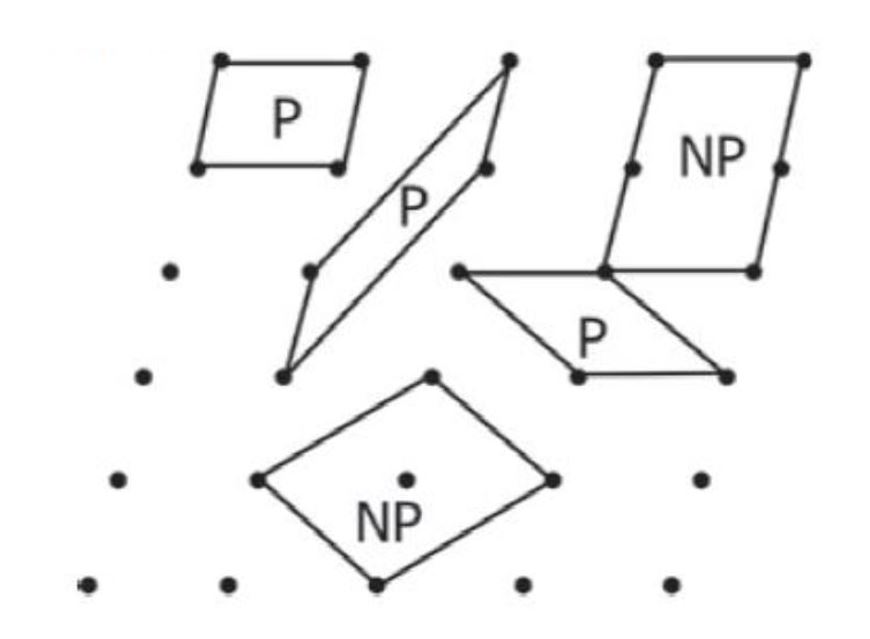
با توجه به ویژگیهای گفته شده در بالا، هر کدام از گزینههای زیر به عنوان سلول واحد را بررسی کنید. کدام یک از سلول واحدها دارای بیشترین تعداد از ویژگیهای مذکور است؟ چرا؟
توضیح: در این شکل "اولیه" بودن یا نبودن سلول واحد با P و NP نمایش داده شده است.
برای مشخص کردن یک سلول واحد از 6 پارامتر استفاده می شود (شکل8).
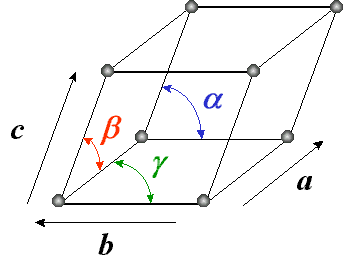
شکل8- نمایش یک سلول واحد با 6 پارامتر [4]
در این میان، a, b, c طول اضلاع و α, β, γ زوایای بین اضلاع هستند. با داشتن این 6 پارامتر میتوان ساختار بلوریهای مختلف را از هم متمایز نمود و هر کدام را باتوجه به سلول واحدش نشان داد.
4- جمعبندی و نتیجهگیری
با بررسی ساختار بلوری یک ماده و تعیین آن میتوان دلیل بسیاری از خواص و ویژگیهای آن را مشخص نمود. برای این منظور از علم بلورشناسی استفاده میشود تا با بررسی حالتهای مختلف بلوری در مواد، قوانین حاکم بر آنها، آرایشهای اتمی یا مولکولی، روشهای مشخصهیابی بلورها و ساخت بلورها اطلاعات ارزشمندی از ویژگیهای ماده به دست آید. کسب اطلاعات از ساختار درونی بلورها در قرن نوزدهم با کشف پرتوایکس قوت گرفت و دوره جدیدی را در بلورشناسی ایجاد نمود. بسته به اینکه مواد دارای ساختار بیشکل باشند یا بلوری، خواص کاملا متفاوتی از خود نشان میدهند. یک ماده بلوری در حالت تکبلور یا چندبلور ویژگیهای متمایزی دارد که تمامی آنها تعیینکننده ساختار بلوری در یک ماده میباشند. برای نشاندادن ساختار بلوری یک ماده میتوان سلول واحد را به نمایندگی از آن ساختار بلوری نمایش داد. سلول واحد دارای 6 پارامتر (اندازه اضلاع و زاویه بین آنها) است که باعث یکتایی آنها میشود. همچنین انتخاب یک سلول واحد نیازمند دارا بودن شرایطی همچون ساده بودن، کوچک بودن، داشتن بیشترین تقارن و اولیه بودن آن سلول واحد است.
5- مراجع
[1]. Callister, William D., and David G. Rethwisch. Materials science and engineering: an introduction. Vol. 7. New York: John wiley & sons, 2007.
[2]. Allen, Samuel M., and Edwin L. Thomas. The structure of materials. Vol. 44. New York: Wiley, 1999.
[3]. Askeland, Donald R., and Pradeep P. Phule. The science and engineering of materials. Pacific Grove/Ca: Brooks/Cole, 2003.
[4]. De Graef, Marc, and Michael E. McHenry. Structure of materials: an introduction to crystallography, diffraction and symmetry. Cambridge University Press, 2012.