یکشنبه 10 اسفند 1399 کد خبر: 86

۱- مقدمه
مدادی که در دست گرفتهاید، لباسی که پوشیدهاید، یا هر آنچه از بدو تولد با آن سروکار داشتهاید و حتی مواد سازنده بدن انسان، همه ماده[۱] هستند. در واقع ما در دنیایی متولد میشویم و رشد میکنیم که مادی است! ازاینرو یکی از راههای اساسی شناخت دنیای پیرامون ما، شناخت صحیح مواد است.
۲- تقسیمبندی مواد از نظر حالت
مواد در شرایط طبیعی معمولاً در سه حالت گاز[۲]، مایع[۳] و جامد[۴] هستند، که با ویژگی های آنها آشنا هستید. در صورت بروز شرایط خاص، ماده وارد حالت چهارم که پلاسما[۵] نام دارد میشود.
پلاسما شباهت بسیاری به حالت گازی ماده دارد؛ زیرا نیروی مؤثر چندانی بین ذرات تشکیلدهندۀ پلاسما که توانایی کنار هم نگه داشتن آنها را داشته باشد وجود ندارد. بااینوجود، تفاوت اصلی میان این دو حالت ماده، در یونیزه بودن ذرات تشکیلدهندۀ پلاسما است. بنابراین، پلاسما از مجموعهای ذرات باردار الکتریکی (با بارهای غیرهمنام) تشکیل شده است که آزادانه در محیط پیرامونی خود حرکت میکنند. ازاینرو میتوان یک گاز را با استفاده از روشهایی که بتواند ذرات تشکیلدهنده آن را یونیزه کند، تبدیل به پلاسما کرد؛ حرارت دادن گاز یا قرار دادن آن در معرض میدان قوی الکتریکی از روشهایی هستند که یک گاز خنثی را تبدیل به پلاسما میکند.
برهمکنشهای بینذرهای به دو دسته درون مولکولی و بین مولکولی تقسیم میشوند. در هر مولکول، اتمها توسط نیروهای درون مولکولی کنار هم نگه داشته شدهاند. این برهمکنشهای درون مولکولی ناشی از نیروهایی است که باعث ایجاد پیوند شیمیایی میان اتمها و در نتیجه تشکیل مولکولها میشوند. پیوند یونی میان ذرات تشکیلدهنده نمک خوراکی (NaCl)، پیوند اشتراکی (کووالانسی) میان اتمهای اکسیژن و کربن در مولکول کربن دیاکسید (CO2) و یا پیوند فلزی میان اتمهای آهن در یک توده آهن نمونههایی از برهمکنشهای درون مولکولی است.
مولکولها در مایعات و جامدات با نیروهای بین مولکولی در کنار یکدیگر قرار میگیرند. این نیروها به صورت نیروهای جاذبه یا دافعه بین مولکولهای نزدیک هم ایجاد میشوند و نسبت به نیروهای درون مولکولی ضعیفتر هستند؛ برای مثال پیوند اشتراکی که درون مولکول آب، بین اتمهای تشکیلدهنده آن وجود دارد بسیار قویتر از نیروی جاذبه (پیوند هیدروژنی) بین مولکول آب و سایر مولکولهای مجاورش است. انواع برهمکنشهای واندروالسی از جمله پیوندهای هیدروژنی، در اثر برهمکنش دوقطبیهای لحظهای و یا دائمی بین مولکولها تشکیل میشود. نیروهای بین مولکولی به دلیل اینکه ماهیت الکتریکی دارند، بسیار کوتاه برد هستند؛ با اینوجود این نیروها در مقیاسهای بزرگ یعنی هنگامی که تعداد بسیار زیادی از ذرات با هم برهمکنش دارند، بسیار تأثیرگذار بوده و تعیینکنندۀ بسیاری از خواص ماده هستند.
مواد جامد را میتوان به دو گروه کلی بیشکل[۶] و بلورین[۷] تقسیمبندی کرد. در مواد بیشکل چیدمان اتمها یا مولکولهای سازنده از هیچ نظم خاصی پیروی نمیکند. درحالیکه مواد بلورین از کنار هم قرار گرفتن اتمها یا مولکولها بهصورت منظم شکل میگیرند. نظم موجود در این مواد دارای دو شرط اصلی است؛ دورهای[۸] (تکرارشونده) و بلند برد است که با گسترش در هر سه جهت فضایی، ساختاری تعریفشده ایجاد میکند که به آن بلور[۹] میگویند. در هر بلور کوچکترین واحد متشکل از اتمها یا مولکولهای سازنده که نظم ساختاری بلور را در خود دارد و بهعنوان الگویی تکرارشونده است، سلول واحد[۱۰] گفته میشود. بر اساس این تعریف، یک ماده جامد بلورین با تکرار سلول واحد آن در سه بعد شکل میگیرد؛ درنتیجه فضا از تکرار سلولهای واحد پر شده و شبکه بلورین[۱۱] را پدید میآورد.
شاخهای از علم مواد که به مطالعۀ ساختار بلوری مواد میپردازد، بلورشناسی[۱۲] نامیده میشود. بنابر مطالعات بلورشناسی تمامی مواد بلورین بر اساس تنوع شکل هندسی سلول واحد، فقط در هفت نوع دستگاه بلوری طبقهبندی میشوند، این هفت دستگاه عبارتند از: مکعبی[۱۳]، چهارگوشه[۱۴]، شش گوشه[۱۵]، راست لوزی[۱۶]، لوزی پهن[۱۷]، تک شیب[۱۸] و سه شیب[۱۹]. با جایگذاری اتمها در این هفت دستگاه، چهارده شبکۀ بلوری حاصل میشود. این شبکههای بلوری چهاردهگانه به افتخار کشف علمی براوه در سال ۱۸۴۸ میلادی به شبکههای براوه[۲۰] معروفاند (شکل ۱). قرارگیری انواع اتمها یا مولکولها در این شبکههای بلوری، بلورهای متنوعی با خواص متمایزی را ایجاد میکند.
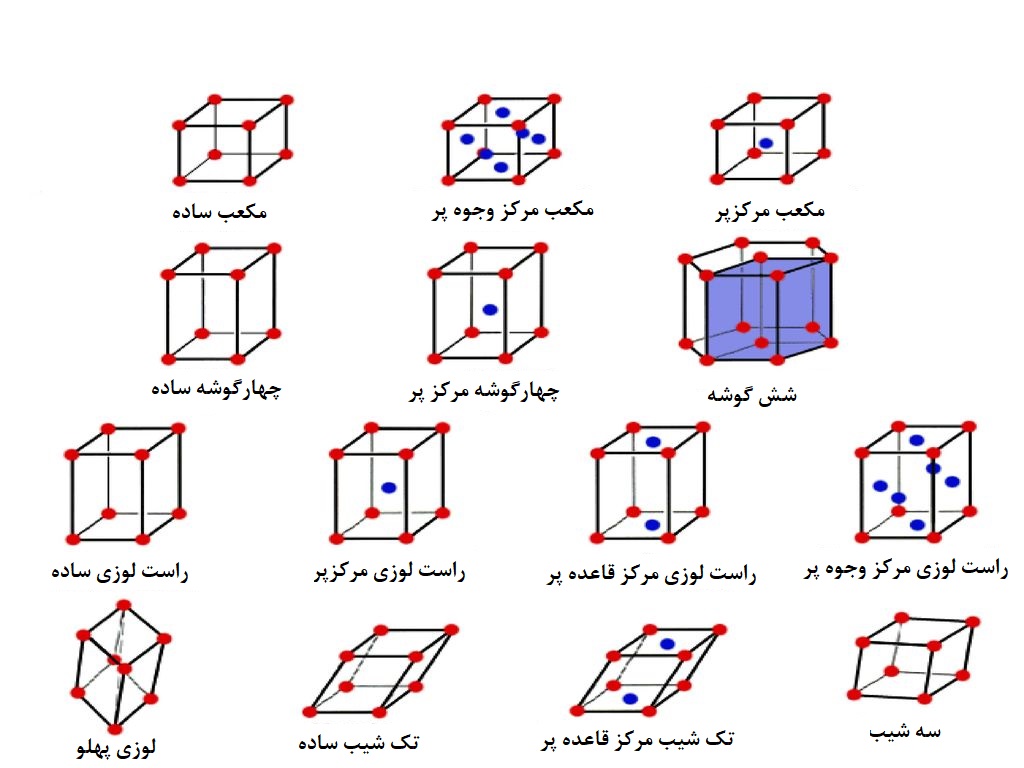
شکل ۱- تصویر ۱۴ شبکۀ براوه در ۷ دستگاه بلوری.
هر سلول واحد با شش عدد مشخصه توصیف میشود؛ این اعداد ششگانه با نام ثابتهای شبکه[۲۱] به اعداد مشخصۀ یک سلول واحد معروفند که در دو گروه جای میگیرند. گروه اول مربوط به طول اضلاع اصلی سلول واحد است و گروه دوم زاویۀ بین این ضلعها را نشان میدهد؛ در شکل ۲ اندازۀ سه ضلع سازنده (a و b و c) و زاویه بین هر دو ضلع سازنده (α و β و γ) نمایش داده شده است. برای مثال در شبکۀ براوه مکعبی، اندازه ضلعها باهم برابرند و زاویه بین آنها ۹۰ درجه است. در شبکۀ سه شیب هیچکدام از سه ضلع اندازه برابر ندارند و زاویه بین هر دو ضلع نیز با زاویههای دیگر متفاوت است (a ≠ b≠ c و γ ≠ β ≠ α).
برای بیان مشخصههای فضایی یک سلول واحد، علاوه بر ثابتهای شبکه، سه مشخصۀ مهم دیگر نیز وجود دارد که عبارتند از: تعداد اتمهای موجود در یک سلول واحد، تعداد همسایگان یک اتم در یک سلول واحد (عدد همسایگی[۲۲]) و جزئی از حجم سلول واحد که توسط اتمها اشغال شده است (ضریب فشردگی[۲۳] اتمی).
در ساختار مکعبی ساده، هر اتم با ۶ اتم دیگر همسایه است، سه اتم در سه گوشۀ مجاور در همان سلول واحد و سه اتم در سلولهای دیگر. این نشان میدهد عدد همسایگی این ساختار برابر شش است.
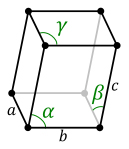
شکل ۲- نحوۀ نشان دادن یک شبکه بلوری و شش متغیر آن.
ضریب فشردگی[۲۴] اتمی میزان پر شدن فضای شبکه توسط اتمها را نشان میدهد و از نسبت حجم اتمهای داخل سلول واحد بر حجم کل سلول واحد به دست میآید (رابطۀ ۱).
 |
رابطه۱ |
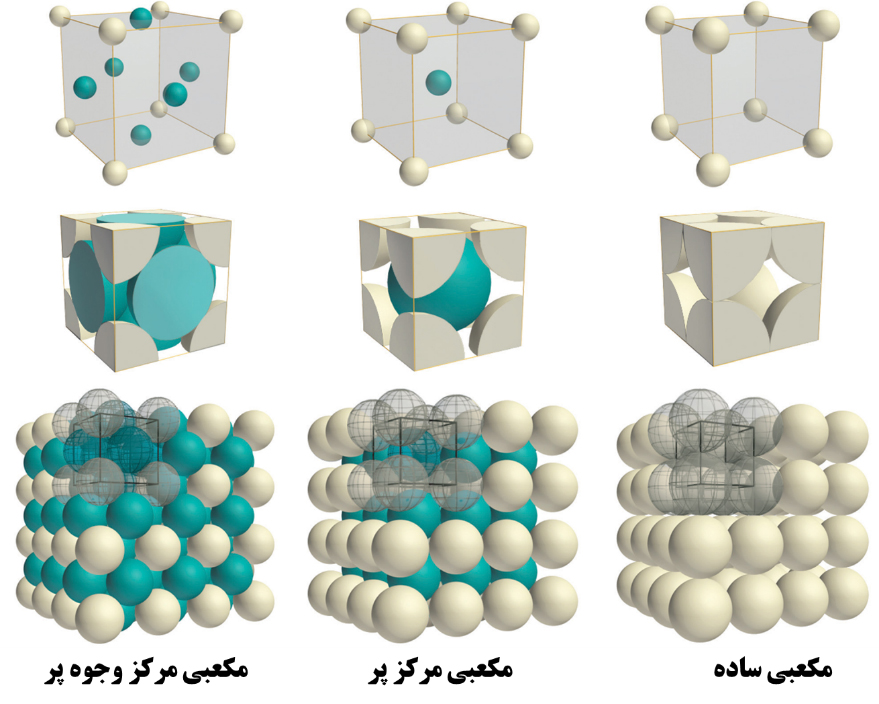
شکل ۳- تصویری از سه نوع ساختار بلوری مکعبی متداول.
در ادامه این مشخصهها را در سادهترین سلول واحد (مکعبی ساده) بررسی میکنیم. ساختار سلول واحد مکعبی ساده را در شکل ۳ در نظر بگیرید. ۸ اتم در ۸ گوشۀ مکعب قرار دارند ولی بهصورت کامل داخل سلول واحد مکعبی نیستند. اگر یکی از این ۸ اتم را در نظر بگیریم، متوجه میشویم که این اتم بین سلول واحد نشان داده شده و ۷ سلول واحد دیگر که در آن گوشه با هم همسایه هستند، مشترک است. پس میتوان گفت فقط آن اتم متعلق به سلول واحد نشان داده شده است؛ درنتیجه تعداد اتمهای سازندۀ یک واحد شبکۀ مکعبی ساده برابر است. از سوی دیگر هر اتم در این ساختار، با ۶ اتم دیگر همسایه است، سه اتم در سه گوشۀ مجاور در همان سلول واحد و سه اتم در سلولهای دیگر؛ از اینرو عدد همسایگی این ساختار برابر شش است. همانطور که در شکل برای ساختار مکعبی قابلمشاهده است، اتمهای مجاور در این ساختار، روی اضلاع مکعب بر هم مماسند. با فرض آنکه در این رابطه R شعاع کرۀ اتم باشد (با تقریب خوبی شکل اتم را کروی کامل فرض کردیم.) اندازه ضلع مکعب سلول واحد دو برابر اندازه شعاع هر اتم است (a = 2R)؛ پس طبق رابطه ۱، ضریب فشردگی ۰/۵۲ محاسبه میشود:
| =ضریب فشردگی ساختار مکعبی ساده |
رابطه ۲ |
با همین روش می توان ضریب فشردگی را برای سه ساختار بلوری مهم دیگر یعنی مکعبی مرکزپر، مکعبی مرکز وجوه پر و ششگوشه فشرده محاسبه نمود. ضریب فشردگی در سلول واحد مکعبی مرکزپر ۰/۶۸، مرکز وجوه پر ۰/۷۴ و ضریب فشردگی سلول واحد هگزاگونال فشرده ۰/۷۴ محاسبه میشود، برای اطلاع از جزئیات این محاسبه میتوانید به کتاب مراجعه نمایید.
صفحههای بلوری[۲۵]، صفحههایی مجازی هستند که حداقل از سه نقطۀ غیر همراستا در شبکه براوه عبور میکنند و محل تقاطع آنها با نقاط در شبکۀ بلور، نظم تعریفشده و تکرارپذیری را به وجود میآورد. در علم بلورشناسی با هدف توصیف بهتر اجزای یک شبکۀ بلوری، این صفحات مفروض شدهاند. در شکل ۴ سه صفحه از میان انواع صفحههای بلوری ممکن برای ساختار بلوری مکعبی ساده نشان داده شده است.
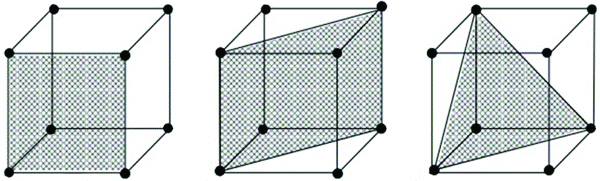 شکل ۴- سه صفحۀ بلوری از میان انواع صفحههای بلوری برای ساختار بلوری مکعبی ساده.
شکل ۴- سه صفحۀ بلوری از میان انواع صفحههای بلوری برای ساختار بلوری مکعبی ساده.
همه صفحههای بلوری مشابه را میتوان با گروهی از اعداد صحیح که موسوم به شاخصهای میلر[۲۶] هستند، توصیف کرد. بهطورمعمول هر دستۀ مشخص از صفحههای بلوری (صفحههای موازی که همارز هستند) را با استفاده از سه عدد صحیح h، k و l نشان میدهند که به شکل (hkl) نوشته میشود. شاخص میلر درواقع نام و نشان یک صفحۀ بلوری است و در مباحث بلورشناسی هر صفحهای با شاخص میلر آن معرفی میشود. سادهترین راه برای به دست آوردن شاخصهای میلر برای صفحههای بلوری، تعیین محل برخورد این صفحهها با محورهای دستگاه مختصاتی است که سلول واحد شبکۀ بلوری موردمطالعه بر آن منطبق است. در چنین دستگاه مختصاتی که در اصطلاح دستگاه مختصات بلورشناسی[۲۷] نامیده میشود، سه بردار یکۀ a1,a2,a3 بهترتیب در راستای محورهای x,y,z تعریف میشوند که طول آنها برابر طول ثابت شبکۀ همراستای آنها بوده و زاویه میان این بردارها نیز برابر زاویۀ شخصۀ سلول واحد است. شکل ۵ تصویری از دستگاه مختصات بلورشناسی برای شبکۀ بلوری مکعبی ساده و مختصات محل قرارگیری اتمهای یک بلور شبکۀ مکعبی ساده در این دستگاه را نشان میدهد.
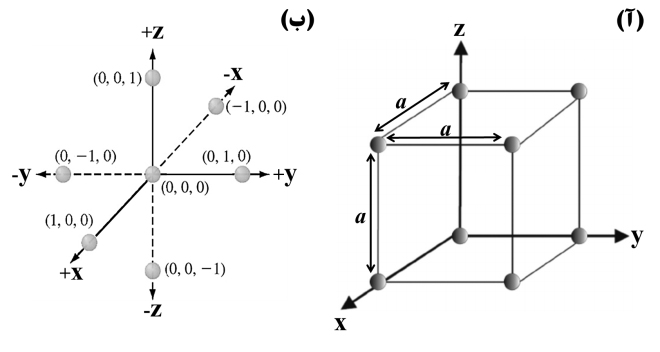 شکل ۵- (آ) شبکۀ بلوری مکعبی ساده با ثابت شبکۀ a در دستگاه مختصات بلورشناسی و (ب) مختصات محل قرارگیری اتمهای یک بلور شبکۀ مکعبی ساده در این دستگاه.
شکل ۵- (آ) شبکۀ بلوری مکعبی ساده با ثابت شبکۀ a در دستگاه مختصات بلورشناسی و (ب) مختصات محل قرارگیری اتمهای یک بلور شبکۀ مکعبی ساده در این دستگاه.
شاخصهای میلر یک صفحۀ بلوری برابر معکوس محل قطع محورهای دستگاه مختصات بلورشناسی توسط آن صفحه است. به اینترتیب که معکوس طول در محل قطع محور x برابر h، معکوس عرض در محل قطع محور y برابر k و معکوس ارتفاع در محل قطع محور z برابر l میباشد. درصورتیکه یک صفحه موازی یک محور باشد، محل قطع برابر بینهایت فرض شده و معکوس بینهایت، صفر است. شکل ۶-آ برای مثال صفحهای را نشان میدهد که هر سه محور دستگاه مختصات بلورشناسی را در محل قرارگیری اتمهای شبکۀ مکعبی ساده قطع میکند؛ مختصات محل را میتوان بهراحتی و با کمک گرفتن از شکل ۵-ب تعیین کرد. طول، عرض و ارتفاع محل قطع محورهای مختصات برابر یک است؛ درنتیجه شاخص میلر این صفحه برابر (111) به دست میآید. شکل ۶-ب صفحهای را نشان میدهد که طول و عرض محل قطع محورهای مختصات آن برابر یک است، درحالیکه این صفحه موازی محور z بوده و در هیچ نقطهای این محور را قطع نمیکند؛ ازاینرو شاخص میلر این صفحه برابر (110) است. به همینترتیب شاخص میلر صفحۀ مشخصشده در شکل ۶-پ (100) میباشد. لازم به ذکر است که در یک دستگاه مختصات بلورشناسی، تمامی صفحههای موازی همارز بوده و با یک شاخص میلر مشخص میشوند.
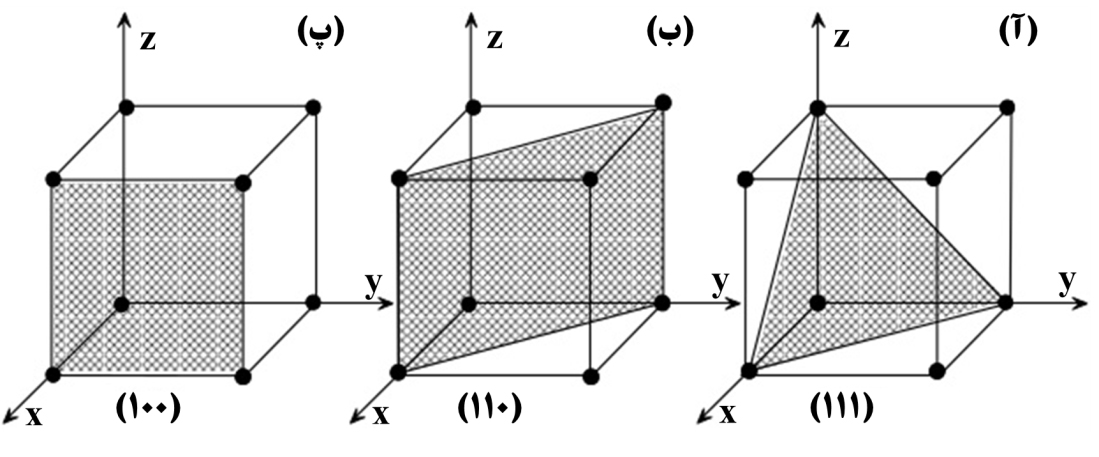 شکل ۶- سه صفحۀ بلوری (111)، (110) و (100) در یک بلور مکعبی ساده.
شکل ۶- سه صفحۀ بلوری (111)، (110) و (100) در یک بلور مکعبی ساده.
ممکن است محل قطع محور مختصات توسط صفحۀ بلوری در نیمۀ منفی آن رخ دهد، در چنین حالتی مؤلفۀ مربوط به این عدد منفی با گذاشتن یک خط تیره بر روی معکوس آن بیان میشود؛ بهعنوان مثال اگر صفحهای دو محور افقی و عمودی (x و z) را در یک و محور عرضی (y) را در منفی یک قطع کند، شاخص میلر آن برابر () خواهد بود. در مواردی که محل قطع یک صفحه کمتر از یک (عددی کسری) باشد، در شاخص میلر چنین صفحهای اعدادی بزرگتر از یک وجود خواهند داشت؛ برای مثال صفحهای که شاخص میلر آن (211) است، محور x را در نقطه ۰/۵ و محور y و z را در نقطه ۱ قطع میکند؛ این شاخص میتواند در شبکۀ بلوری مکعبی مرکزپر، منسوب به صفحهای باشد که دربردارندۀ دو اتم مستقر بر روی محورهای y و z و اتم موجود در مرکز سلول واحد است (شکل ۷).
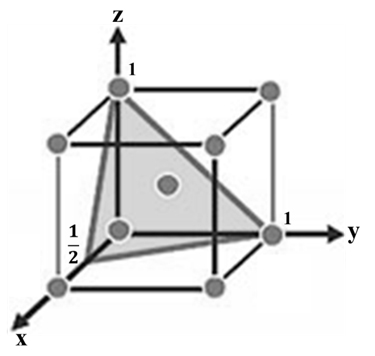 شکل ۷- نمایش یک صفحه بلوری با شاخص میلر (211) در شبکه بلوری مکعبی مرکزپر.
شکل ۷- نمایش یک صفحه بلوری با شاخص میلر (211) در شبکه بلوری مکعبی مرکزپر.
کشف تغییرات قابلتوجهی که در خواص مواد در ابعاد نانو رخ میدهد، سبب شده است که در سالهای اخیر مواد جامد را در دو گروه اصلی تودهای[۲۸] و نانویی[۲۹] نیز تقسیمبندی کنند.
بر این اساس، نانوماده به مادهای گفته میشود که حداقل یکی از ابعاد آن (طول، عرض و ارتفاع) در ابعاد نانو باشد، به این معنی که ابعاد آن در محدودۀ ۱-۱۰۰ نانومتر باشد و یا از اجزای مؤثری با این اندازه تشکیل شده باشد. لازم به ذکر است همه اتمها و بسیاری از مولکولهای معمولی با وجود آنکه اندازهای بسیار کوچک دارند (کمتر از ۱ نانومتر)، در دسته نانومواد قرار نمیگیرند.
از زمانهای قدیم، انسانها از نانومواد برای درمان (طب سنتی چینی) و تولید رنگها (روم باستان) استفاده میکردند. همچنین، نانوموادی مانند جوهر رنگارنگ و جادویی، که از نانوذرات[۳۰] کلوئیدی[۳۱] ساخته شده بود، در کارهای هنری استفاده میشد؛ برای مثال در جام لیکرگوس[۳۲] و شیشههای رنگی کوچک و بزرگ استفادهشده در تزئین کلیساها، ردپایی از نانوذرات فلزی وجود دارد. بااینحال، ما نمیدانیم که آیا در آن دوران انسان علم دقیقی به ماهیت این نانومواد و خواص منحصربهفرد آنها داشته است یا خیر!
 شکل ۸- جام لیکرگوس در زیر نور معمولی به رنگ سبز یشمی و درصورت تابانده شدن نور از داخل آن، قرمز یاقوتی دیده میشود. شیشۀ جام لیکرگوس حاوی مقدار کمی ذرات نقره و طلا با قطری در حدود ۵۰ نانومتر (کمتر از یکهزارم یک دانۀ نمک) است [۱].
شکل ۸- جام لیکرگوس در زیر نور معمولی به رنگ سبز یشمی و درصورت تابانده شدن نور از داخل آن، قرمز یاقوتی دیده میشود. شیشۀ جام لیکرگوس حاوی مقدار کمی ذرات نقره و طلا با قطری در حدود ۵۰ نانومتر (کمتر از یکهزارم یک دانۀ نمک) است [۱].
پس از معرفی نانومواد، اکنون زمان آن رسیده تا تعریف دقیق علم نانو[۳۳] ارائه شده و مفهوم فناوری نانو[۳۴] بیان شود. رایجترین تعریف علم نانو به این صورت بیان میشود:
علم نانو به مطالعه پدیدهها در ابعاد نانو میپردازد؛ از سویی سعی در کشف خواص مواد در این ابعاد دارد و از سوی دیگر به دنبال توجیه و درک این خواص نوظهور با خلق نظریات جدید و بهرهگیری از نظریات موجود میباشد. دانشمندان علم نانو همواره با تبیین اصول حاکم بر حوزه نانو بهرهبرداری از خواص نانومواد را برای مهندسین نانو ممکن میسازند.
تمامی مواد و اجسام در پیرامون ما سه بعد طول، عرض و ارتفاع دارند. در نانومواد حداقل یکی از این ابعاد سهگانه در محدوده نانو قرار دارد. ازاینرو دستهبندی نانومواد بر اساس تعداد ابعاد نانویی آنها انجام میشود؛ نانوموادی که هر سه بعد آنها در محدودۀ نانو کمترباشد، نانومواد صفربعدی؛ نانوموادی که دو بعد آنها در محدودۀ نانو باشد، نانومواد یکبعدی و آنهایی که تنها یک بعد در محدودۀ نانو دارند، نانومواد دوبعدی نامیده میشوند. در واقع در این تقسیمبندی از ابعاد نانویی در مقابل ابعاد دیگر صرفنظر میشود.
در دستهبندی نانومواد گروه دیگری از نانومواد به نام نانومواد سهبعدی نیز وجود دارند. این نانومواد هیچ بعدی در محدودۀ نانو ندارند و در تمامی ابعاد سهگانه دارای ابعادی بهمراتب بزرگتر از محدودۀ نانومواد هستند. آنچه مواد تودهای را تبدیل به نانوماده سهبعدی میکند وجود اجزای سازندۀ نانویی است که بهصورت مستقیم در خواص آنها مادۀدخیل هستند؛ بهعنوان مثال ماده مرکبی[۳۵] که جزء تقویتکننده آن یک نانوماده یکبعدی یا صفر بعدی باشد، خود یک نانوماده سهبعدی است و یا پارچهای که به الیاف آن نانوذرات ضد باکتری افزوده شده است، نیز نانومواد سهبعدی به شمار میآید. علاوه بر اجزای نانویی، وجود خلل و فرج نانویی نیز مادۀ تودهای را به نانوماده سهبعدی تبدیل میکند. شکل (۹) طرحی بسیار ساده از این 4 گروه از نانومواد را نشان میدهد.
 شکل ۹- دستهبندی چهارگانۀ نانومواد بر اساس ابعاد هندسی آنها.
شکل ۹- دستهبندی چهارگانۀ نانومواد بر اساس ابعاد هندسی آنها.
نانومواد صفربعدی، معروفترین نانوساختارهای مورد استفاده هستند که معمولاً با نام نانوذرات شناخته میشوند. اندازه نانوذرات در هر سه بعد کوچکتر از ۱۰۰نانومتر است. این نانومواد هم بهصورت بیشکل و هم بهصورت بلورین و در انواع شکلها از جمله کروی، مکعبی، هرمی، پوسته کروی، هسته-پوسته[۳۶] و غیره وجود دارند. شکل نانوذرات تابع روش تولید و شرایط محیطی تهیه آنها است و روی خواص و حوزه کاربردیشان تأثیر دارد. شکل ۱۰ طرحی از چند نوع نانومادۀ صفر بعدی را نشان میدهد.
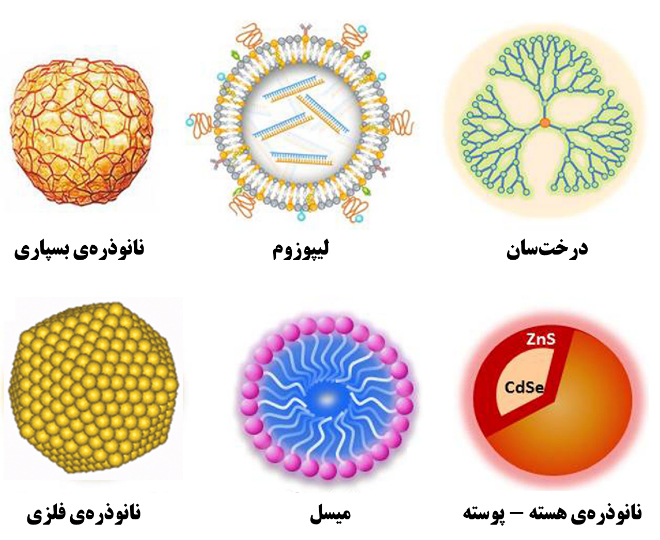 شکل ۱۰- طرحی از چند نمونه از نانومواد صفربعدی؛ طرح بر اساس مرجع شماره [۲].
شکل ۱۰- طرحی از چند نمونه از نانومواد صفربعدی؛ طرح بر اساس مرجع شماره [۲].
نقاط کوانتومی[۳۷] از مهمترین نانومواد صفربعدی هستند که ساختار بلوری داشته و نیمهرسانا میباشند. نقاط کوانتومی در دمای محیط معمولاً اندازهای در حدود ۱۰نانومتر دارند انواع ترکیبهای نیمهرسانا مانند ZnSe، CdSe و CdTe ازجمله مواد مورد استفاده برای تولید نقاط کوانتومی هستند. ویژگیهای نوری منحصربهفرد این نانومواد صفربعدی موجب کاربرد فراوان آنها در حوزههایی مانند الکترونیک، اپتیک و پزشکی شده است [۳]. از آنجا که هر نقطه کوانتومی وابسته به اندازه خود طیف انرژی[۳۸] مجزایی دارد، بعد از قرار گرفتن در معرض تابش نور، تنها میتواند یک طولموج مشخص تکرنگ را منتشر کند (شکل ۱۰-آ). از اینرو انتشار رنگهای مختلف از نقاط کوانتومی در اندازههای مختلف و در شرایط یکسان تابش نور، حیرت آور است. دلیل این رفتار در بخش بعدی بهطور کامل بررسی خواهد شد.
فولرنها[۳۹] از جذابترین نانومواد صفربعدی هستند که ساختاری شبیه به یک توپ توخالی دارند (به همین دلیل به آنها Buckyball هم گفته میشود). اتمهای کربن در ساختار فولرنها با پیوندهای اشتراکی در پنجضلعیها و ششضلعیهایی به هم وصل شدهاند و ساختاری قفس مانند را تشکیل دادهاند. معروفترین فولرن شناختهشده، فولرن C60 است که دارای ۲۰ ششضلعی و ۱۲ پنجضلعی است. فولرن C60 خواص زیستی جالبی داشته و کاربرد آن در فرآیندهای درمانی و پزشکی که از فناوری نانو و مواد نانوساختار استفاده میشود در حال گسترش است (شکل ۱۱- ب).
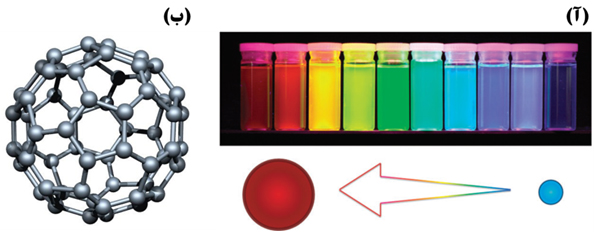
شکل ۱۱- (آ) تغییر رنگ نشر شده توسط نقاط کوانتومی با تغییر اندازۀ آنها [۴] و (ب) طرحی از ساختار یک فولرن C60.
نانومواد یکبعدی، نانوساختارهایی هستند که دو بعد آنها حتماً در محدوده نانو قرار دارد و طول بعد دیگر حداقل چندین برابر دو بعد نانومتری است. نانومواد یکبعدی با توجه به شکل ظاهری و نسبت طول به سطح مقطع آنها، در چهار گروه اصلی نانوالیاف[۴۰]، نانوسیمها[۴۱]، نانومیلهها[۴۲] و نانولولهها[۴۳] دستهبندی میشوند. به نسبت طول بعد بزرگتر به طول بعد کوچکتر اصطلاحاً نسبت ابعادی یا نسبت منظر[۴۴] گفته میشود. نانوسیم یا نانولیف، نانومادهای است که نسبت ابعادی آن بسیار بزرگ (عددی در بازه ۱۰۰ الی ۱۰۰۰) است. اگر نسبت ابعادی در محدود ۱۰ الی ۱۰۰ باشد، به آن نانوماده یکبعدی، نانومیله گفته میشود و همانطور که از نام نانولولهها برداشت میشود، نانولولهها نانومواد یکبعدی توخالی هستند (شکل ۱۲).
 شکل ۱۲- تصویر میکروسکوپ الکترونی روبشی از (آ) نانوسیمهای سیلیکون [۵] (ب) نانوالیاف پلیاتیلن اکسید [۶] و (پ) نانولولههای تیتانیوم دیاکسید [۷].
شکل ۱۲- تصویر میکروسکوپ الکترونی روبشی از (آ) نانوسیمهای سیلیکون [۵] (ب) نانوالیاف پلیاتیلن اکسید [۶] و (پ) نانولولههای تیتانیوم دیاکسید [۷].
خواص منحصربهفردی همچون رسانایی الکتریکی و خواص نوری، مغناطیسی، حسگری و زیستی، سبب شده که نانومواد یک بعدی کاربردهای بسیاری در تمامی صنایع از جمله در صنعت الکترونیک پیداکنند. یکی از جالبترین ویژگی نانومواد یکبعدی، رفتار الکترونیکی آنها و تغییرات هدایت الکتریکی آنها است. یکبعدی بودن این نانوساختارها موجب میشود که حرکت الکترونها صرفاً در راستای محور آنها ممکن باشد. برای نانولولههای کربنی[۴۵] که بهعنوان یکی از مهمترین نانوساختارهای یکبعدی به شمار میروند، حرکت محوری الکترونها شکل خاصی به خود میگیرد که به آنترابرد بالستیک الکترون[۴۶] گفته میشود. به این معنی که الکترونها میتوانند بدون ممانعت فضایی در راستای محور نانولوله حرکت کنند. این امر موجب میشود نانولولههای رسانا توانایی رسانش جریان الکتریکی در حدود ۱۰۰۰ برابر بیشتر از فلز مس را داشته باشند.
بااینحال برخی مشاهدات تجربی و نیز مفاهیم فیزیکی حاکی از آن است که رسانش الکتریکی نانوسیمهای فلزی از حالت تودهای آنها کمتر است؛ زیرا هنگامی که قطر سیم کمتر از طول پویش آزاد الکترونها[۴۷] است، الکترونها در مرزهای پیرامونی نانوسیمها پراکنده میشوند. در این شرایط کاهش قطر نانوسیم موجب کاهش طول پویش آزاد الکترون شده و کاهش رسانایی سیم را در پی خواهد داشت. دومین عاملی که خواص الکتریکی نانوسیمها را بهشدت تحت تأثیر قرار میدهد، پدیدهای موسوم به اثر لبه[۴۸] است. این پدیده از اتمهایی که در سطح نانوسیمها حضور دارند نشأت میگیرد؛ این اتمهای سطحی به دلیل اینکه بهطور کامل به اتمهای مجاور خود متصل نیستند، رفتاری متفاوت از اتمهای درونی داشته و ازآنجاییکه عامل بسیاری از عیوب ساختاری در نانوسیمها هستند، موجب کاهش رسانایی نانوسیمها نسبت به حالت تودهای آنها میشوند. بااینحال وجود این اتمهای سطحی برای نانوسیمها یک مزیت به شمار میرود و کاربرد ارزشمند استفاده بهعنوان نانوحسگر را برای نانوسیمها در پی دارد. بهاینترتیب که با جذب اولین اتم یا مولکول بر روی سطح یک نانوسیم، رسانایی الکتریکی آن تغییر بسیار محسوسی میکند که با آشکارسازی آن، میتوان به وجود گونه جدید در محیط پی برد.
یکی دیگر از ویژگیهای مهم نانوسیمها این است که در صورت کاهش ابعاد سطح مقطع نانوسیم نیمهرسانا به مقادیری کمتر از ۲۰ نانومتر، این نانوسیم اثرات کوانتومی از خود نشان میدهد؛ ازاینرو به آن، سیم کوانتومی[۴۹] گفته میشود. رسانایی الکتریکی سیمهای کوانتومی کوانتیزه است؛ بهاینترتیب که الکترونهایی که از نانوسیم عبور میکنند صرفاً دارای مقادیر گسستهای از انرژی میباشند.
از دیگر نانوساختارهای یکبعدی پرکاربرد میتوان به نانوالیاف اشاره کرد. الیاف به مواد جامدی گفته میشود که در عین انعطافپذیری و ظرافت بالا، طول بسیار بلندتری نسبت به قطرشان (بیش از ۱۰۰۰ برابر) دارند. حال اگر قطر این الیاف محدود به ابعاد نانومتری شود، این مواد نانوالیاف نامیده میشوند. امروزه نانوالیاف در بسیاری از حوزهها بهویژه در صنایع دارویی، مهندسی بافت، زخم پوششها، صنایع نساجی، ساخت فیلترها و فرآیندهای جداسازی کاربرد دارند. کشسانی (مقاومت کششی) بالا، نسبت سطح به حجم بسیار بالا و طول بسیار زیاد از ویژگیهایی است که نانوالیاف را منحصربهفرد و کاربردی میسازد.
نانومواد دوبعدی گروهی دیگر از نانوساختارها هستند که یک بعد از آنها در ابعاد نانو قرار دارد و طول دو بعد دیگر چندین برابر بزرگتر از طول بعد کوچکتر است. نانومواد دوبعدی بهصورت ذاتی دو نوع مختلف دارند؛ یا بهصورت مستقل در قالب نانوصفحهها[۵۰] یا نانوورقهها[۵۱] هستند یا بهصورت لایۀ نازک[۵۲] روی زیرلایههای[۵۳] مختلف رشد داده میشوند.
لایههای نازک یا نانوپوششها با ضخامت نانومتری روی سطح یک مادۀ دیگر به نام زیرلایه قرار میگیرند. مهمترین کاربرد نانولایهها، ایجاد ویژگیهای سطحی موردنیاز مثل آبگریزی، مقاومت به خوردگی، مقاومت به سایش و غیره روی زیرلایه است. لایههای نازک کاربردهای گستردهای در ساخت ادوات الکترونیکی و تجهیزات نوری دارند؛ همچنین از لایههای نازک بهعنوان پوششهایی با کاربردهای ضدسایش و ضدخوردگی نیز استفاده میشود. شبیه به نانوذرات و نانومواد یکبعدی، در نانولایهها نیز اگر ضخامت نانولایه نیمهرسانا به حدی کم باشد که اثرات کوانتومی مشاهده شود، به آنها لایهنازک چاه کوانتومی[۵۴] گفته میشود.
 شکل ۱۳- تصویر میکروسکوپ الکترونی روبشی از نانولایههای گرافیتی با ضخامت نانومتری تهیهشده از طریق لایهلایه کردن مغز مداد [۸].
شکل ۱۳- تصویر میکروسکوپ الکترونی روبشی از نانولایههای گرافیتی با ضخامت نانومتری تهیهشده از طریق لایهلایه کردن مغز مداد [۸].
دسته دیگر نانومواد دوبعدی، نانوصفحهها و نانوورقهها هستند که مستقل از زیرلایهاند. از مهمترین نانوصفحهها میتوان نانوصفحههای گرافن[۵۵] را نام برد. گرافن یک تکلایه از اتمهای کربن است که گرافیت از روی هم قرار گرفتن تعداد زیادی از این تکلایهها تشکیل شده است (شکل ۱۳). گرافن به دلیل خواص منحصربهفردی مانند رسانایی الکتریکی فوقالعاده زیاد، شفافیت، پایداری شیمیایی و استحکام مکانیکی بالا امروزه توجه بسیاری از دانشمندان را به خود جلب کرده است.
مواد سهبعدی نانوساختار یا نانومواد تودهای یا حجیم، دستهای از نانومواد هستند که ابعاد ظاهری بزرگتری از محدودۀ تعریف فناوری نانو دارند. آنچه که باعث میشود این گروه از مواد جزء نانومواد دستهبندی شوند این است که برخی از اجزای سازنده آنها حداقل یک بعد نانومتری دارند و یا دارای تخلخل نانومتری هستند. نانومواد سهبعدی در حالت کلی شامل مواد نانوترکیب[۵۶]، مواد نانومتخلخل[۵۷] (دارای حفرههای نانومقیاس) و مواد نانوبلوری[۵۸] یا نانومواد ریزدانه میباشد.
مواد نانوترکیب: مواد مرکب[۵۹]، موادی هستند که از دو یا چند جزء مختلف و قابلتفکیک تشکیل شدهاند. در مواد مرکب جزء اصلی که بخش اعظم ماده را تشکیل میدهد، به زمینه[۶۰] معروف است؛ جزء دوم که اصطلاحاً با نام تقویتکننده[۶۱] شناخته میشود، با هدف تقویت خواص ماده زمینه در آن پراکنده میشود. در برخی موارد جزء سومی نیز به زمینه اضافه میشود که نقش چندانی در بهبود خواص ندارد و صرفاً برای افزایش حجم و کاهش هزینۀ تولید نهایی به زمینه افزوده میشود، به این جزء پرکن[۶۲] گفته میشود. هدف از افزودن اجزای دیگر به مادۀ زمینه در مواد مرکب، تغییر یا بهبود خواص ماده زمینه و به دست آوردن مادهای ترکیبی با خواص دلخواه و بهبود یافته است.
سادهترین و قدیمیترین مادۀ مرکب ساخته شده به دست بشر کاهگل است. حال اگر یکی از اجزای یک مادۀ مرکب در ابعاد نانو باشد (انواع نانومواد صفر بعدی، یکبعدی و دو بعدی)، مادۀ مرکب حاصل را ماده مرکب نانویی یا در اصطلاح مادۀ نانوترکیب مینامند. بهطورمعمول در مواد نانوترکیب جزء تقویتکنندهای که به زمینه اضافه میشود، یک مادۀ نانوساختار است. بهبود خواص در مواد مرکب نانویی بسیار چشمگیرتر از مواد مرکب معمولی است؛ دلیل این امر برهمکنش بسیار قوی انواع نانومواد استفادهشده بهعنوان تقویتکننده در ساخت مواد نانوترکیب است.
مواد نانومتخلخل: موادی که تخلخل[۶۳] آنها (نسبت حجم فضای خالی ماده به حجم ظاهری ماده) بین ۲۰% تا ۹۵% باشد، مواد متخلخل[۶۴] نامیده میشوند. مواد نانومتخلخل دارای حفرههایی در ابعاد نانو (قطر کمتر از ۱۰۰نانومتر) بوده و بخش قابلتوجهی از حجم آنها را فضای خالی تشکیل میدهد. وجود حفرههای بسیار ریز و مرتبط به هم موجب ایجاد سطح ویژۀ (نسبت سطح به جرم) بسیار زیادی در مواد نانومتخلخل میشود. از مهمترین خواص مواد نانومتخلخل میتوان به سطح ویژه بسیار بالا، نفوذپذیری یا تراوایی بالا و عایق بودن در برابر گرما و صوت اشاره کرد.
مواد نانومتخلخل بر اساس اندازه حفرهها به سه گروه مواد ریز حفره[۶۵] (دارای حفرههایی با قطر کمتر از ۲نانومتر)، مواد متوسط حفره[۶۶] (دارای حفرههایی با قطر ۲-۵۰ نانومتر) و مواد درشت حفره[۶۷] (دارای حفرههایی با قطر بیشتر از ۵۰نانومتر) تقسیمبندی میشوند. مواد نانومتخلخل در زمینههای بسیاری کاربرد دارند؛ استفاده از این نوع نانومواد در انواع فیلتر و غشا، تصفیۀ آب، عایق صوتی و حرارتی، کاتالیست و پایهی کاتالیست، ذخیرهسازی هیدروژن و حامل دارو ازجملهی کاربردهای گستردۀ مواد نانومتخلخل است. انواع آیروژلها[۶۸]، زئولیتها[۶۹] و اکسید آلومینیوم آندایز شده (AAB)[۷۰] از شناختهشدهترین مواد نانومتخلخل هستند [۹].
نانومواد ریزدانه: تمامی مواد از اتمها یا یونها تشکیل شدهاند. اگر این اجزای سازنده با نظم و الگوی مشخص کنار یکدیگر قرار گرفته باشند (نظم دوربرد و تکرارشونده)، ماده دارای نظم بلوری خواهد بود، در غیر این صورت ماده بیشکل است. در شرایط واقعی غالباً این نظم ساختاری در مواد بلورین سراسری نبوده و کل ماده را در بر نمیگیرد؛ بلکه ماده از ذرات کوچکتری که در هر کدام این نظم بلوری وجود دارد، تشکیل شده است؛ برای مثال یک شاخه نبات را در نظر بگیرید (شکل ۱۴-آ)، این قطعۀ نبات از تعداد زیادی دانههای[۷۱] بلورین متصلبههم تشکیل شده است. نوع نظم ساختاری (شبکۀ بلور) در تمامی این دانهها یکسان است و صرفاً جهتگیری این دانههای بلوری کوچک نسبت به هم متفاوت است. محل اتصال این دانهها که در اصطلاح مرزدانه[۷۲] نامیده میشود، فاقد ساختار بلوری بوده و محل گذار جهت نظم بلوری از دانهای به دانۀ دیگر است (شکل ۱۴-ب). چنین ساختارهایی که از اتصال تعداد زیادی دانههای بلورین به هم شکل گرفتهاند را مواد چند بلوری[۷۳] مینامند. بااینوجود این امکان وجود دارد که یک جسم صرفاً از یک بلور تشکیل و دربردارندۀ هیچ دانهای نباشد. چنین موادی را مواد تکبلور[۷۴] مینامند. دانهبندی نهتنها در مواد حجیم دیده میشود بلکه در نانومواد نیز وجود دارد. بهعنوان مثال، نانوذرات ممکن است خود از چندین دانه تشکیل شده باشند.

شکل ۱۴- (آ) تصویری از یک شاخه نبات و (ب) طرحی از مرز دانهها در یک مادۀ چندبلوری.
 شکل ۱۵- تصویر میکروسکوپ نوری از دانهبندی یک قطعه فلز تیتانیوم [۱۰]
شکل ۱۵- تصویر میکروسکوپ نوری از دانهبندی یک قطعه فلز تیتانیوم [۱۰]
بسیاری از موادی که در اطراف ما وجود دارد مواد چندبلوری هستند؛ از جمله انواع فلزات. شکل ۱۵ تصویر میکروسکوپی از دانههای یک قطعه تیتانیوم را نشان میدهد؛ در این تصویر مرز دانهها بهخوبی قابلمشاهده است. اتمهای موجود در مرز یک دانه متعلق به هیچکدام از دانهها نیستند؛ مرز دانهها نوعی نقص بلوری به شمار میآند که تأثیر زیادی روی خواص فیزیکی مواد چندبلوری دارند.
سومین گروه اصلی نانومواد حجیم، مواد نانوبلورین یا نانومواد ریزدانه هستند که ابعاد دانهها در این مواد در محدوده نانومتری است. اگر ابعاد دانهها در مواد چندبلوری کمتر از ۱۰۰نانومتر باشد، به آنها مواد نانوبلورین گفته میشود. ریزدانه شدن مواد چند بلوری موجب بهبود چشمگیر برخی از خواص مکانیکی آنها ازجمله استحکام آنها میشود؛ ازاینرو امروزه مواد نانوبلورین مورد توجه قرار گرفتهاند.
۸- مراجع
[1]. Lycurgus Cup: A Piece of Ancient Roman Nanotechnology. December 2018; Available from: https://www.amusingplanet.com/2016/12/lycurgus-cup-piece-of-ancient-roman.html.
[2]. Mc Carthy, D.J., et al., Nanoparticles and the Blood-Brain Barrier: Advancing from In-Vitro Models Towards Therapeutic Significance. Pharmaceutical Research, 2015. 32(4): p. 1161-1185.
[3]. Zaman, M., et al., Nanoparticles in relation to peptide and protein aggregation. International Journal of Nanomedicine, 2014. 9(1): p. 899-912.
[4]. Zrazhevskiy, P., M. Sena, and X. Gao, Designing multifunctional quantum dots for bioimaging, detection, and drug delivery. Chemical Society Reviews, 2010. 39(11): p. 4326-4354.
[5]. Goldberger, J., et al., Silicon Vertically Integrated Nanowire Field Effect Transistors. Nano Letters, 2006. 6(5): p. 973-977.
[6]. Panda, P.K. and S. Ramakrishna, Electrospinning of alumina nanofibers using different precursors. Journal of Materials Science, 2007. 42(6): p. 2189-2193.
[7]. Sun, K.-C., et al., Synthesis and characterization of highly ordered TiO2 nanotube arrays for hydrogen generation via water splitting. Materials Chemistry and Physics, 2011. 129(1): p. 35-39.
[8]. Graphene Discovery Leads to Top Physics Prize. 2006 December 2018; Available from: https://www.photonics.com/Articles/Graphene_Discovery_Leads_to_Top_Physics_Prize/a27116.
[9]. Karuppiah, J., E.L. Reddy, and Y.S. Mok, Anodized aluminum oxide supported NiO-CeO2 catalyst for dry reforming of propane. Catalysts, 2016. 6(10).
[10]. Zhu, C., et al., Investigation of the shear response and geometrically necessary dislocation densities in shear localization in high-purity titanium. International Journal of Plasticity, 2017. 92: p. 148-163.
۹- پاورقیها
|
1. |
Matter |
26. |
Miller indices |
51. |
Nanosheet |
|
2. |
Gas |
27. |
Crystallographic systems |
52. |
thin film |
|
3. |
Liquid |
28. |
Bulk |
53. |
Substrate |
|
4. |
Solid |
29. |
Nanomaterial |
54. |
Quantum well |
|
5. |
Plasma |
30. |
Nanoparticle |
55. |
graphene |
|
6. |
Amorphous |
31. |
Colloid |
56. |
Nanocomposite material |
|
7. |
Crystalline |
32. |
Lycurgus cup |
57. |
Nanoporous material |
|
8. |
Periodic |
33. |
Nanoscience |
58. |
Nanocrystalline material |
|
9. |
Crystal |
34. |
Nanotechnology |
59. |
Composite |
|
10. |
Unit cell |
35. |
Composite |
60. |
Matrix |
|
11. |
Crystal lattice |
36. |
Core-shell |
61. |
Reinforcement |
|
12. |
Crystallography |
37. |
Quantum Dot |
62. |
Filler |
|
13. |
Cubic |
38. |
Energy Spectrum |
63. |
Porosity |
|
14. |
Tetragonal |
39. |
Fullerene |
64. |
Porous |
|
15. |
Hexagonal |
40. |
Nanofiber |
65. |
Microporous |
|
16. |
Orthorombic |
41. |
Nanowire |
66. |
Mesoporous |
|
17. |
Rombohedral |
42. |
Nanorod |
67. |
Macroporous |
|
18. |
Monoclinic |
43. |
Nanotube |
68. |
Aerogel |
|
19. |
Triclinic |
44 |
Aspect ratio |
69. |
Zeolite |
|
20. |
Bravais lattice |
45. |
Carbon nanotube (CNT) |
70. |
Anodized aluminum oxide |
|
21. |
Lattice constants |
46. |
Ballistic electron transport |
71. |
Grain |
|
22. |
Coordination Number (CN) |
47. |
electron mean free path |
72. |
Grain boundary |
|
23. |
Atomic Packing Factor (APF) |
48. |
Edge effect |
73. |
Polycrystalline |
|
24. |
Packing factor |
49. |
Quantum wire |
74. |
Single crystal |
|
25. |
Lattice plane |
50. |
Nanoplate |
|
|