سهشنبه 07 مرداد 1404 کد خبر: 177
۱-هدف
خودچیدمانی را به عنوان فرآیندی شناخته میشود که طی آن مولکولها و سلولها تحت شرایط مناسب، خود را به ساختارهای خاص و منظمی تبدیل میکنند.
۲- مقدمه
خودچیدمانی (self assembly) چیست؟ خیلی سادهاش میشود همدیگر را گرفتن. تعریف علمیتر آن عبارت است از این که خودچیدمانی یک روش ساخت از پایین به بالاست که در آن، اتمها یا مولکولها، یا ارتباطات فیزیکی و شیمیایی، خود را به شکل یک ساختار منظم نانویی در میآورند. ایجاد بلور نمک یا دانههای برف با آن ساختارهای پیچیده، مثال خوبی برای خودچیدمانی است. حالا تصور کنید، یک پازل دستتان باشد و آن را به شدت تکان دهید و پس از بهم ریختن پازل، ببینید که پازل خود به خود در حال درست شدن است. میبینید چه تصور عجیبی است؟! اما چنین اتفاقی در طبیعت چندان عجیب نیست. خیلی از سیستمهای بیولوژیکی و سیستمهای فیزیکی غیر آلی، رفتارهای خودچیدمانی را به خوبی نمایش میگذارند.
۳- تئوری آزمایش:
پیشرفتهای علمی جدید، به متخصصان نانوفناوری توانایی جابجایی و چیدمان اتمها را داده است. اگرچه این یک شاهکار شگفتانگیز است، اما همچنان فرآیند ساخت مواد نانومقیاس از مواد ماکرومقیاس یک راه حل زمانبر و غیرعملی است. برای سادهسازی این فرآیند، دانشمندان در حال آزمایش فرآیندی به نام خودچیدمانی هستند.
خودچیدمانی که در طبیعت رایج است، فرآیندی است که طی آن مولکولها و سلولها خود را به ساختارهای کارآمد سازماندهی میکنند. این اتفاق میلیونها بار در روز و به روشهای مختلف رخ میدهد. در واقع، همه موجودات زنده، از جمله انسانها، حاوی ساختارهایی هستند که خودچیدمانی میشوند. یک مثال بارز در انسان، ساخت DNA است. کدها و توالیهای ژنتیکی فرآیند خودچیدمانی را هدایت میکنند که تحت شرایط خاص رخ میدهد.
متخصصان نانوفناوری از خودچیدمانی برای تولید سریع و ارزان نانومواد استفاده میکنند. ترفند خودچیدمانی در درک چگونگی تأثیر شرایط خاص مانند دما و فشار بر نحوه تعامل مولکولها نهفته است، زیرا این شرایط اغلب برای هر فرآیند خودچیدمانی منحصر به فرد هستند. دانشمندان میتوانند از تمایلات طبیعی مولکولها برای پیوند در الگوهای بسیار خاص تحت شرایط خاص، برای ساخت ساختارهای کوچکتر، پیچیدهتر و با مقادیر بیشتر استفاده کنند.
۱-۳-یکی از کاربردهای خودچیدمانی:
خودچیدمانی به طور گسترده در ساخت نانوکپسولها مورد استفاده قرار میگیرد. نانوکپسول به هر نانوذرهای گفته میشود که دارای یک پوسته خارجی و یک فضای داخلی توخالی متناظر باشد. این کپسولها که از نظر اندازه متفاوت هستند که از میلیونها نانوذره ساخته شدهاند. فضای داخلی را میتوان با تعدادی از مواد مختلف پر کرد. این نانوکپسولها که به عنوان "داروهای هوشمند" نیز شناخته میشوند، میتوانند برای ایجاد یک سیستم دارورسانی هدفمندتر استفاده شوند. کپسولها با گیرندههای شیمیایی خاصی ساخته میشوند که فقط به سلولهای خاص متصل میشوند. این پیشرفت به دارو اجازه میدهد تا بدون تأثیر بر سلولهای سالم، مستقیماً به سلولهای بیمار برسد. همچنین امکان کاهش دوز دارو را فراهم میکند زیرا مستقیماً به منبع مورد نیاز میرسد. این امر میتواند منجر به کاهش 10000 برابری دوز دارو شود. با چنین کاهشی، عوارض جانبی مضر درمانهایی مانند شیمیدرمانی میتواند تا حد زیادی به حداقل رساند.
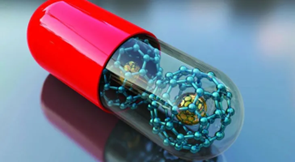
شکل ۱-نانو کپسول
۴- روش کار آزمایش
آلژینات سدیم با فرمول شیمیایی (C6H7NaO6)n شناخته شده و به صورت رشتههایی سفید تا قهوهای و یا در فرم دانهای، پودری و گرانولی به خرید و فروش میرسد. آلژینات سدیم یک پلیمر طبیعی است که از جلبکهای قهوهای استخراج میشود و به عنوان یک افزودنی غذایی و در صنایع دیگر کاربرد دارد. این ماده به دلیل خواص ژلسازی، امولسیونکنندگی و افزایش ویسکوزیته، در صنایع مختلفی از جمله صنایع غذایی، داروسازی و آرایشی بهداشتی مورد استفاده قرار میگیرد.
کاربرد آلژینات سدیم در صنایع داروسازی:
تولید قرص و کپسول: آلژینات سدیم به عنوان یک عامل اتصالدهنده و روکشدهنده در تولید قرصها و کپسولها استفاده میشود.
تولید ژلهای دارویی: به عنوان یک حامل دارو و در تولید ژلهای دارویی کاربرد دارد.
پانسمان زخم: آلژینات سدیم در پانسمانهای زخم به دلیل خاصیت جذب ترشحات و ایجاد محیط مرطوب برای بهبود زخم استفاده میشود.
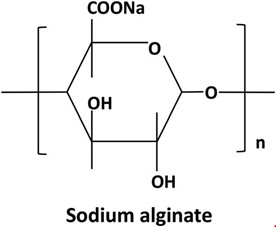
شکل ۲- ساختار مولکولی سدیم آلرژینات
کلسیم کلرید خوراکی به فرمول شیمیایی CaCl2 یک ترکیب شیمیایی است که به عنوان یک افزودنی در صنایع غذایی استفاده میشود. شکل ظاهری کلسیم کلرید به صورت پودر سفید، بدون بو و رطوبت است. بسته به نیاز افراد در اشکال مختلف (گلوله، پوسته پوسته یا گرانول) عرضه میشود. وقتی در آب حل شود، یک محلول شفاف و بی رنگ تولید میکند. این ترکیب در آب، الکل، پیریدین و متانول قابل حل و در آمونیاک، دی متیل سولفوکسید و اتیل استات نامحلول است.
این ماده به دلیل خاصیت سفت کنندگی، جذب رطوبت و تنظیم pH کاربرد دارد. همچنین به عنوان یک منبع کلسیم در نوشیدنیها و مکملهای غذایی مورد استفاده قرار میگیرد.
۱-۴- مواد و تجهیزات مورد نیاز
آلژینات سدیم خوراکی
کلرید کلسیم خوراکی یا ( نمک خوراکی)
استیرر یا مخلوطکن (در صورت انجام آزمایش در خانه)
چهار کاسه ( آلژینات، آب، کلرید کلسیم و آب شستشو)
طعم دهنده خوراکی
رنگ خوراکی
صاف کننده
قطره چکان یا سرنگ بدون سوزن
خط کش
۲-۴- روش انجام آزمایش
نصف قاشق چایخوری پودر آلژینات سدیم و ۱ فنجان آب را در مخلوط کن بریزید. تا زمانی که پودر آلژینات سدیم کاملاً حل شود، مخلوط کنید.
۴ قاشق غذاخوری طعم دلخواه را اضافه کنید. دوباره مخلوط کنید. (اگر قطرهها درحمام پخش شدند یا ته نشین شدند، محلول آلژینات خیلی رقیق بوده و کمی پودرآلژینات بیشتری الزم دارد.)
بگذارید ۱۵ تا ۳۰ دقیقه بماند تا حبابهای هوا خارج شوند
دو و یک چهارم فنجان آب گرم را در یک کاسه بزرگ یا ظرف پلاستیکی بریزید. ۴/۳ قاشق چایخوری کلرید کلسیم را در آب حل کنید و هم بزنید.
یک پیپت یا سرنگ بدون سوزن را با محلول آلژینات پر کنید.
چند قطره در کاسه آب بریزید صافی را داخل محلول کلرید کلسیم قرار دهید.
در حالی که صافی در حمام کلرید کلسیم غوطهور است، به آرامی قطرات کوچکی از محلول آلژینات را داخل صافی بریزید.
هنگامی که مایع ژل در تماس با آب نمک قرار میگیرد، در نتیجه واکنش شیمیایی یک نوع پلیمر ایجاد میشود. یک پلیمر، از زنجیرههای بزرگ مولکولی تشکیل شده است که در واحدهای بسیار زیاد تکرار شدهاند. این پلیمر دیواره خارجی اشکال جالب را تشکیل میدهد. در حقیقت در تماس با آب نمک، یک لایه پلیمری در سطح خارجی ایجاد میشود.
نتایج: دانههای آلژینات سدیم بلافاصله پس از برخورد با محلول کلرید کلسیم تشکیل میشوند.
توجه: قبل از مصرف، دانهها را در حمام آب تمیز بشویید.
۵- پرسش
۱-چه اتفاقی در مرحله آخر آزمایش می افتد؟
۲-اگر آلژینات سدیم را در سود حل کنیم بعد آزمایش انجام شود چه تغییری مشاهده میشود؟
منابع:
۱-کتاب بچههای دانشمند جلد۱
۲-https://www.nisenet.org/nanodays