یکشنبه 01 بهمن 1402 کد خبر: 166
سنتز نانوذرات سیلیکا با ابعاد حدود ۱۰۰ نانومتر به روش اشتوبر.
سیلیکا با ثابت الکتریک ۴/۵ به سبب پایداری فوقالعاده در برابر لختهشدن، مادهای پرکاربرد برای سنتز ساختارهای هسته-پوسته است؛ همچنین بیاثر بودن سیلیکا از حیث شیمیایی، شفافیت و صورت نگرفتن واکنشهای اکسایش-کاهش در سطح آن، از دیگر دلایل جذابیت این ماده است.
برای سنتز نانوذرات سیلیکا از روش اشتوبر که در سال ۱۹۶۸ ارائه شد استفاده میشود. این روش شامل هیدرولیز (یک فرآیند تجزیه شیمیایی که در آن از آب برای گسستن پیوندهای شیمیایی یک ماده استفاده میشود.) تترا اتیل اورتو سیلیکات در بستری از اتانول در حضور آمونیوم هیدروکسید است. در این روش از آمونیوم هیدروکسید به عنوان کاتالیزور استفاده میشود. طی سنتز نانوذرات سیلیکا، واکنشهای زیر رخ میدهند:
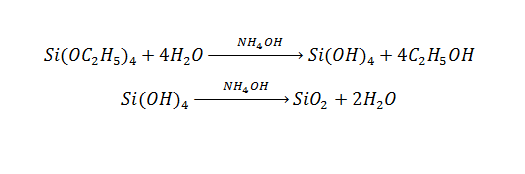
مرحله اول سنتز نانوذرات سیلیکا، شامل هیدرولیز تترا اتیل اورتو سیلیکات و جانشینی یونهای هیدروکسید به جای گروههای عاملی اتیل است.
طی مرحله دوم که بسپارش تراکمی نامیده میشود، سیلیسیم هیدروکسید در حضور کاتالیزور به سیلیکا تبدیل میگردد و محلولی شیریرنگ حاصل میشود.
قطر نانوذرات سیلیکا با تغییر غلظت تترا اتیل اورتو سیلیکات و آمونیوم هیدروکسید از ۵۰ نانومتر تا ۱ میکرون متغیر است. با کاهش غلظت تترا اتیل اورتو سیلیکات، قطر نانوذرات نیز کاهش مییابد.
با افزایش غلظت آمونیم هیدروکسید، قطر ذرات ابتدا افزایش و سپس کاهش مییابد.
دلیل افزایش اولیه، افزایش سرعت هیدرولیز تترا اتیل اورتو سیلیکات در حضور کاتالیست است ولی به تدریج با افزودن آمونیوم هیدروکسید، سرعت تراکم از سرعت هیدرولیز بیشتر شده و اندازه ذرات کاهش مییابد. میزان مصرف کاتالیزور علاوه بر اندازه ذرات بر تخلخل و مورفولوژی آنها نیز تاثیرگذار است.
از جمله موارد قابل بررسی در سنتز نانوذرات سیلیکا، بارسطحی این این ذرات است. در شکل ۱ تغییرات بار سطحی نانوذرات سیلیکا نسبت به pH سیال نشان داده شده است. با توجه به نمودار، بار سطحی نانوذرات سیلیکا در pH بیشتر از ۲، منفی است.
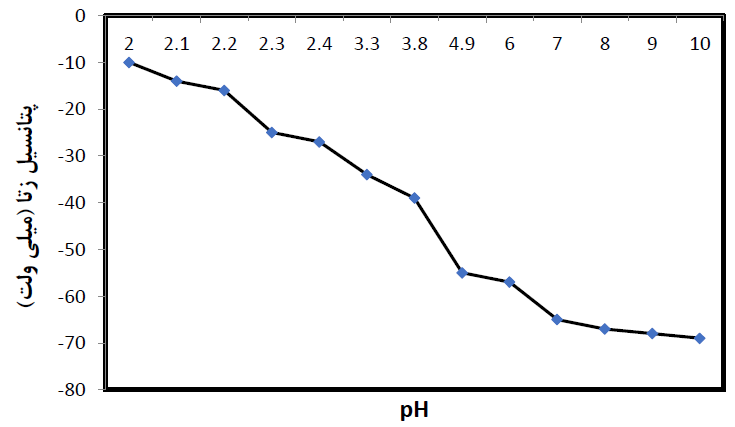
شکل۱- تغییرات بار سطحی نانوذرات سیلیکا نسبت به ph محیط
مواد: محلول تترا اتیل اورتو سیلیکات، محلول آمونیاک، اتانول، آب مقطر.
تجهیزات: ترازوی دیجیتالی، pHمتر، همزن مکانیکی، بالن دودهانه، استوانه مدرج، پیپت مدرج، هاتپلیت استیرر، اولتراسونیک، سانتریفیوژ، هود آزمایشگاهی، دماسنج.
۸/۵ میلیلیتر آمونیوم هیدروکسید، ۵ میلیلیتر آب مقطر و ۱/۵ میلیلیتر تترا اتیل اورتو سیلیکات را در بشری حاوی ۱۰۰ میلیلیتر اتانول افزوده و در دمای ۴۰ درجه سلسیوس به مدت ۳ ساعت هم زده میشوند.
حدود ۲۰ دقیقه پس از شروع اختلاط، محلول تغییر رنگ میدهد و از بیرنگ به محلولی شیریرنگ تبدیل میشود که نشاندهنده تشکیل نانوذرات سیلیکاست.
اندازه نانوذرات به دست آمده در حدود ۱۰۰ نانومتر است. با تغییر مقدار تترا اتیل اورتو سیلیکات به ۲/۵ میلیلیتر، نانوذرات سیلیکا با قطر متوسط ۲۵۰ نانومتر به دست میآید.
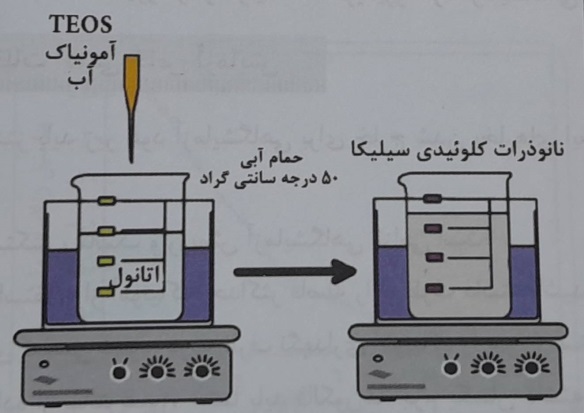
شکل۲- نمای انجام آزمایش
برای تعیین ابعاد ذرات و شکل آنها از میکروسکوپ الکترونی، برای تعیین توزیع اندازه ذرات از دستگاه DLS و برای تعین بار سطحی نانوذرات سنتزشده در شرایط مختلف از دستگاه آنالیز Zeta potential استفاده میشود.
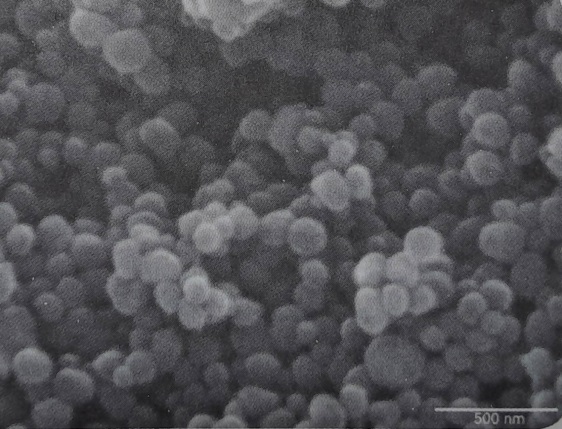
شکل۳- تصویر میکروسکوپی الکترونی(SEM) نانوذرات سیلیکا
مراحل سنتز باید زیر هود آزمایشگاهی برای خارج شدن بخارهای ایجادشده انجام شود.
داشتن دستکش، ماسک و روپوش آزمایشگاهی الزامی است.
در هنگام استفاده از آمونیاک، حداکثر فاصله را از ظرف داشته باشید تا بخارات آن وارد مجاری تنفسی نشود.
درب ظرف نگهداری آمونیاک را پس از استفاده ببندید.
برای استفاده از سانتریفیوژ، حتما باید فالکونها جرم یکسان داشته باشند و صرفا حجم یکسان ملاک نیست.
-با تغییر بار سطحی به سبب تغییرات pH پایداری کلوئید سیلیکا به چه شکلی خواهد بود؟
-پایداری کلوئید سیلیکا سنتزشده، چه مدت است؟ (با مشاهده عینی میتوان نظر داد.)